题目内容
19.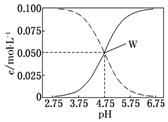 常温下,醋酸、醋酸钠混合溶液中,已知c(CH3COOH)+c(CH3COO-)=0.1mol•L-1,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关溶液中离子浓度关系的说法正确的是( )
常温下,醋酸、醋酸钠混合溶液中,已知c(CH3COOH)+c(CH3COO-)=0.1mol•L-1,溶液中c(CH3COOH)、c(CH3COO-)与pH的关系如图所示.下列有关溶液中离子浓度关系的说法正确的是( )| A. | pH=5.75的溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | pH=7,c(Na+)=0.1 mol•L-1,c( CH3COOH)>c(Na+)=c( CH3COO-)>c(H+)=c(OH-) | |
| C. | pH=3.5的溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1 mol•L-1 | |
| D. | 向W点所表示的1.0 L溶液中通入0.05 mol HCl气体(溶液体积变化可忽略):c(H+)=c(CH3COOH)+c(OH-) |
分析 由图象可看出,浓度增大的曲线应为c(CH3COO-),浓度减小的曲线应为c(CH3COOH),W点时c(CH3COOH)=c(CH3COO-),结合溶液的电荷守恒、物料守恒解答该题.
解答 解:A.pH=5.75比4.75大,W点时c(CH3COOH)=c(CH3COO-),从曲线来看当pH=5.75时,c(CH3COOH)<c(CH3COO-),故A错误;
B.pH=7,溶液存在电荷守恒,应为c(Na+)+c(H+)=c(CH3COO-)+c(OH-),则c(Na+)=c( CH3COO-)>c(H+)=c(OH-),已知c(CH3COOH)+c(CH3COO-)=0.1mol•L-1,所以c(Na+)=c( CH3COO-)<0.1 mol•L-1,故B错误;
C.pH=3.5溶液中c(Na+)+c(H+)=c(CH3COO-)+c(OH-),再把题干中的c(CH3COOH)+c(CH3COO-)=0.1mol•L-1代入即可得c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1 mol•L-1,故C正确;
D.向W点所表示的1.0 L溶液中通入0.05 mol HCl气体,溶液中溶质为0.1mol•L-1的CH3COOH和0.05mol•L-1的NaCl,溶液中的氢离子由醋酸和水电离,所以c(H+)=c(CH3COO-)+c(OH-),故D错误.
故选C.
点评 本题属于基本概念与理论的考查,落点在水解与电离平衡、物料守恒和电荷守恒、离子浓度大小比较.溶液中存在水解与电离两个过程的离子浓度大小比较是考试热点内容,学习中要反复加强训练,题目难度中等.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
10.通常人们把拆开1mol某化学键所吸收的能量或形成lmol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(△H)已知
则下列热化学方程式不正确的是( )
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能 | 436kJ/mol | 243kJ/mol | 431kJ/mol |
| A. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=-91.5kJ/mol | |
| B. | H2(g)+Cl2(g)═2HCl(g)△H=-183kJ/mol | |
| C. | $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g)△H=+91.5kJ/mol | |
| D. | 2HCl(g)═H2(g)+Cl2(g)△H=+183 kJ/mol |
7.表中的数据是破坏1mol物质中的化学键所消耗的能量(kJ):
相同条件下,X2(X代表Cl、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,放出热量最多的是( )
| 物质 | Cl2 | Br2 | I2 | H2 | HCl | HI | HBr |
| 键能/(kJ•mol-1) | 243 | 193 | 151 | 436 | 431 | 298 | 366 |
| A. | Cl2 | B. | Br2 | C. | I2 | D. | 无法判断 |
4.下列有关丙烯酸(CH2=CHCOOH)的说法正确的是( )
| A. | 丙烯酸使溴水褪色属于氧化反应 | |
| B. | 丙烯酸能发生加成反应但不能发生取代反应 | |
| C. | 丙烯酸分子中所有碳原子不可能处于同一平面 | |
| D. | 反应CH2=CHCOOH+H2$→_{△}^{Ni}$CH3CH2COOH的原子利用率为100% |
11.下列与化学概念有关的说法正确的是( )
| A. | Na2O、CaO、Al2O3均为碱性氧化物 | |
| B. | 水玻璃、漂白液、液氯均为混合物 | |
| C. | 氨水能够导电,所以氨水是电解质 | |
| D. | 有单质参加或生成的化学反应不一定是氧化还原反应 |
8.下列反应的离子方程式书写正确的是( )
| A. | 钠和硫酸铜溶液反应:2Na+Cu2+═Cu2+2Na+ | |
| B. | 工业上将Cl2通入石灰乳中制漂白粉:Cl2+2OH-═Cl-+ClO-+H2O | |
| C. | 向Ba(OH)2溶液中加入少量的NH4HSO4溶液:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 1.0mol/L的NaAlO2溶液和2.5mol/L的盐酸等体积混合2AlO2-+5H+═Al3++Al(OH)3↓+H2O |
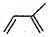 )是合成天然橡胶的单体.请回答下列问题:
)是合成天然橡胶的单体.请回答下列问题: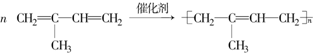 ,该反应类型为加聚反应.
,该反应类型为加聚反应.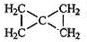 .
.