题目内容
下列离子方程式书写正确的是( )
| A、钠投入水中:Na+H2O=Na++OH-+H2↑ |
| B、将铝投入足量的氨水:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| C、NaHCO3中加入盐酸:HCO3-+H+=CO2↑+H2O |
| D、钠与CuSO4溶液反应:2Na+Cu2+=2Na++Cu |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成NaOH和氢气,电子不守恒;
B.Al与氨水不反应;
C.反应生成氯化钠、水、二氧化碳;
D.反应生成氢气、氢氧化铜、硫酸钠.
B.Al与氨水不反应;
C.反应生成氯化钠、水、二氧化碳;
D.反应生成氢气、氢氧化铜、硫酸钠.
解答:
解:A.钠投入水中的离子反应为2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B.氨水为弱碱溶液,与Al不反应,不能写离子反应,故B错误;
C.NaHCO3中加入盐酸的离子反应为HCO3-+H+=CO2↑+H2O,故C正确;
D.钠与CuSO4溶液反应的离子反应为2Na+2H2O+Cu2+=2Na++Cu(OH)2↓+H2↑,故D错误;
故选C.
B.氨水为弱碱溶液,与Al不反应,不能写离子反应,故B错误;
C.NaHCO3中加入盐酸的离子反应为HCO3-+H+=CO2↑+H2O,故C正确;
D.钠与CuSO4溶液反应的离子反应为2Na+2H2O+Cu2+=2Na++Cu(OH)2↓+H2↑,故D错误;
故选C.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意电子、电荷守恒的应用,选项BD均为解答的易错点,题目难度不大.

练习册系列答案
相关题目
将pH=3的硫酸溶液和pH=10的氢氧化钠溶液相混合,若要使混合后溶液的pH=7,则硫酸溶液和氢氧化溶液的体积比约为( )
| A、1:2 | B、1:9 |
| C、1:10 | D、1:20 |
下列操作或叙述正确的是( )
| A、配制1mol?L-1NaOH溶液时,将溶解后的NaOH溶液立即注入容量瓶 | ||
| B、用小刀切下一小块金属钠,将剩余的钠再放回原试剂瓶 | ||
C、向某溶液中加入BaCl2溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有S
| ||
| D、向沸水中逐滴滴加1mol?L-1FeCl3溶液,并不断用玻璃棒搅拌,可制得Fe(OH)3胶体 |
下列反应,属于复分解反应的是( )
| A、CaCO3═CaO+CO2↑ |
| B、2HClO═2HCl+O2↑ |
| C、NaOH+HCl═NaCl+H2O |
| D、Fe+CuSO4═FeSO4+Cu |
大气层中的臭氧层(O3)能吸收太阳光中的紫外线,下列关于O3的分类正确的是( )
| A、化合物 | B、单质 |
| C、氧化物 | D、混合物 |
下列各组中的两种物质作用时,反应条件或反应物的用量比改变,生成的化合物不会改变的是( )
| A、钠与氧气 |
| B、氢氧化钠与二氧化碳 |
| C、过氧化钠与水 |
| D、氯化铝与氢氧化钠 |
下列关于晶体与非晶体的说法不正确的是( )
| A、区别晶体与非晶体最可靠的科学方法是对固体进行x-射线衍射实验 |
| B、非晶体中粒子的排列无序,所以非晶体具有各向异性 |
| C、晶体有自范性 |
| D、非晶体无固定熔点 |
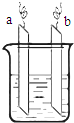 图中,两电极上发生的电极反应分别为:a极:Ag++e-=Ag;b极:Fe-2e-=Fe2+下列说法不正确的是( )
图中,两电极上发生的电极反应分别为:a极:Ag++e-=Ag;b极:Fe-2e-=Fe2+下列说法不正确的是( )| A、a、b可能是同种电极材料 |
| B、该装置一定是电解池 |
| C、装置中电解质溶液一定含有Ag+ |
| D、装置中发生的反应方程式一定是Fe+2Ag+═Fe2++2Ag |
对于反应3Fe(s)+4H2O(g)?Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是( )
A、K=
| ||
B、K=
| ||
| C、增大c(H2O)或减小c(H2),会使该反应平衡常数减小 | ||
| D、改变反应的温度,平衡常数不一定变化 |