��Ŀ����
4�� NO��NO2 ��CO��Ϊ������Ⱦ������������ܹ�ע����ش��������⣺
NO��NO2 ��CO��Ϊ������Ⱦ������������ܹ�ע����ش��������⣺I����Һ���շ�
��1��NaOH��Һ�ɽ�NO��NO2�Ļ������ת��ΪNaNO2���÷�Ӧ�����ӷ���ʽΪNO+NO2+2OH-=2NO2-+H2O��
��2��25��ʱ��HNO2�ĵ��볣��Ka=4.6��10-4�������£���NaNO2��Һ�еμ���������Һ��pH=3ʱ����Һ��$\frac{c��HN{O}_{2}��}{c��N{O}_{2}^{-}��}$=2.2��������λ��Ч���֣�
����֪�ۺ�����NO��CO��ԭ��Ϊ
i.2NO��g��+2CO��g��?N2��g��+2CO2 ��g����H=-746.5kJ•mol-1
ii��C��s��+2NO��g��?N2��g��+CO2 ��g����H=+172.5kJ•mol-1
��3�������£�1mol C��s����CO2 ��ȫ��Ӧ����CO���Ȼ�ѧ����ʽΪC��s��+CO2��g��?2CO��g����H=+919.0kJ/mol��
��4��һ�������£�ij�ܱ������з�����Ӧi�ͷ�Ӧii���ﵽƽ��������������䣬�����¶ȣ�CO��������������������С������Ӱ�족����
��5��һ�������£������ܱ������з�����Ӧi������ʼ��������ϱ�$\frac{c��CO��}{c��NO��}$=y��NO��ƽ��ת���ʣ�a����y���¶ȣ�T���Ĺ�ϵ��ͼ��ʾ��
��y1��y2���������������=����
��M���N���Ӧ�ĸ÷�Ӧ���ʣ�M��N���������������=����
��6��t��ʱ�����ݻ�Ϊ10L�ĺ�ѹ�ܱ������м���1mol C��s����2molNO��g����������Ӧii��5min�ﵽƽ��ʱ�����0��5min�ڣ���CO2��ʾ�ĸ÷�Ӧ����v��CO2��=0.016mol•L-1•min-1��N2���������Ϊa����
��t��ʱ���÷�Ӧ��ƽ�ⳣ��K=4��
���������������䣬��ʼ��������а�������ȼ������ʣ��ﵽƽ��ʱ��N2�����������Ϊa����B��C����ѡ����ĸ��
A.0.5molC��2mol NO B.2mol N2��2mol CO2
C.1mol C��1mol N2��1mol CO2 D.1mol C��1mol NO��1mol N2��
���� I����1��NaOH��Һ�ɽ�NO��NO2�Ļ������ת��ΪNaNO2����ӦΪ������ԭ��Ӧ��ע����ƽ���ݴ�д����Ӧ�����ӷ���ʽ��
��2��25��ʱ��HNO2�ĵ��볣��Ka=4.6��10-4�����뷽��ʽΪ��HNO2?H++NO2-������ƽ�ⳣ������ʽΪKa=$\frac{c��{H}^{+}��c��N{O}_{2}^{-}��}{c��HN{O}_{2}��}$�������£���NaNO2��Һ�еμ���������Һ��pH=3ʱ���ݴ˷������㣻
II����3�������£�1mol C��s����CO2 ��ȫ��Ӧ����CO�ķ���ʽΪ��C��s��+CO2��g��?2CO��g�����÷�Ӧ������֪���Ȼ�ѧ����ʽ�Ƶ������ݸ�˹���ɼ���÷�Ӧ���ʱ䣻
��4��һ�������£�ij�ܱ������з�����Ӧi�ͷ�Ӧii����Ӧi���ȣ���Ӧii���ȣ��ﵽƽ��������������䣬�����¶ȣ�ʹ��Ӧi��ƽ�������ƶ�����Ӧii��ƽ�������ƶ���CO�������ࣻ
��5����һ�������£������ܱ������з�����Ӧi��2NO��g��+2CO��g��?N2��g��+2CO2 ��g��������ͼ���ÿ��Ʊ�����������ȡ��ͬ�¶��£���Ӧ��ʼͶ������ϱ�$\frac{c��CO��}{c��NO��}$=y�����ڿ��淴Ӧ�������������з�Ӧ���������ʹ��һ�ַ�Ӧ���ת�������ݴ˷����жϣ�
��M���N�����ʼ������ͬ������ͼ��M���¶ȴ���N���¶ȣ������¶ȣ�����������Ӧ���ʻ����淴Ӧ���ʣ���������
��6����t��ʱ�����ݻ�Ϊ10L�ĺ�ѹ�ܱ������м���1mol C��s����2molNO��g����������Ӧii��C��s��+2NO��g��?N2��g��+CO2 ��g�����÷�Ӧ��ƽ�ⳣ��ΪK=$\frac{c��C{O}_{2}��c��{N}_{2}��}{{c}^{2}��NO��}$����֪��CO2��ʾ�ĸ÷�Ӧ����v��CO2��=0.016mol/��L•min�����ݴ˼��㣻
���������������䣬��ʼʱ����ͬ�����ϱ�Ͷ�뷴Ӧ���ﵽƽ��ʱ��N2�����������Ϊa���䣬��ϵ�Чƽ���֪ʶ������
��� �⣺I����1��NaOH��Һ�ɽ�NO��NO2�Ļ������ת��ΪNaNO2����ӦΪ������ԭ��Ӧ����Ӧ�����ӷ���ʽΪ��NO+NO2+2OH-=2NO2-+H2O��
�ʴ�Ϊ��NO+NO2+2OH-=2NO2-+H2O��
��2��25��ʱ��HNO2�ĵ��볣��Ka=4.6��10-4�����뷽��ʽΪ��HNO2?H++NO2-������ƽ�ⳣ������ʽΪKa=$\frac{c��{H}^{+}��c��N{O}_{2}^{-}��}{c��HN{O}_{2}��}$�������£���NaNO2��Һ�еμ���������Һ��pH=3ʱ����ʱ��Һ��c��H+��=10-3mol/L��
������Һ��$\frac{c��HN{O}_{2}��}{c��N{O}_{2}^{-}��}$=$\frac{c��{H}^{+}��}{{K}_{a}}$=$\frac{1{0}^{-3}}{4.6��1{0}^{-4}}$=2.2��ע�Ᵽ����λ��Ч���֣�
�ʴ�Ϊ��2.2��
II����֪����2NO��g��+2CO��g��?N2��g��+2CO2 ��g����H1=-746.5kJ/mol��
��C��s��+2NO��g��?N2��g��+CO2 ��g����H2=+172.5kJ/mol��
��3�������£�1mol C��s����CO2 ��ȫ��Ӧ����CO�Ļ�ѧ����ʽΪ��C��s��+CO2��g��?2CO��g�����÷�Ӧ���ɢ�-�ٵõ������ݸ�˹���ɣ��÷�Ӧ���ʱ�Ϊ��H=��H2-��H1=172.5-��-746.5��=+919.0kJ/mol��
���Ը÷�Ӧ���Ȼ�ѧ����ʽΪ��C��s��+CO2��g��?2CO��g����H=+919.0kJ/mol��
�ʴ�Ϊ��C��s��+CO2��g��?2CO��g����H=+919.0kJ/mol��
��4��һ�������£�ij�ܱ������з�����Ӧi�ͷ�Ӧii����Ӧi���ȣ���Ӧii���ȣ��ﵽƽ��������������䣬�����¶ȣ�ʹ��Ӧi��ƽ�������ƶ�����Ӧii��ƽ�������ƶ���CO�������࣬��CO�������������
�ʴ�Ϊ������
��5����һ�������£������ܱ������з�����Ӧi��2NO��g��+2CO��g��?N2��g��+2CO2 ��g��������ͼ���ÿ��Ʊ�����������ȡ��ͬ�¶��£���Ӧ��ʼͶ������ϱ�$\frac{c��CO��}{c��NO��}$=y�����ڿ��淴Ӧ�������������з�Ӧ���������ʹ��һ�ַ�Ӧ���ת��������Ҳ����CO������y��ֵ����NO��ƽ��ת�����������ϣ�y����NO��ƽ��ת����������ͼ����y1��y2��
�ʴ�Ϊ������
��M���N�����ʼ������ͬ������ͼ��M���¶ȴ���N���¶ȣ������¶ȣ�����������Ӧ���ʻ����淴Ӧ���ʣ�����������M���N���Ӧ�ĸ÷�Ӧ����ΪM��N��
�ʴ�Ϊ������
��6����t��ʱ�����ݻ�Ϊ10L�ĺ�ѹ�ܱ������м���1mol C��s����2molNO��g����������Ӧii��C��s��+2NO��g��?N2��g��+CO2 ��g�����÷�Ӧ��ƽ�ⳣ��ΪK=$\frac{c��C{O}_{2}��c��{N}_{2}��}{{c}^{2}��NO��}$����֪��CO2��ʾ�ĸ÷�Ӧ����v��CO2��=0.016mol/��L•min����5min�ﵽƽ��ʱ����CO2���ĵ���Ϊ��c��CO2��=v��CO2����t=0.08mol/L�����ݷ�Ӧ����ʽ��������c��CO2��=0.08mol��c��N2��=0.08mol��ƽ��ʱ��c��NO��=0.2mol/L-2��0.08mol/L=0.04mol/L����t��ʱ���÷�Ӧ��ƽ�ⳣ��ΪK=$\frac{0.08mol/L��0.08mol/L}{��0.04mol/L��^{2}}$=4��
�ʴ�Ϊ��4��
���������������䣬��ʼʱ����ͬ�����ϱ�Ͷ�뷴Ӧ���ﵽƽ��ʱ��N2�����������Ϊa���䣬�ɿ��Ƿ�Ӧ�ǵ�Чƽ��ģ�ԭƽ���ǰ�1mol C��s����2molNO��g����������ܱ�������Ӧ�ģ��÷�Ӧ���������غ�ķ�Ӧ����������֮�£����Чƽ��Ϊ��ʼʱ��1molN2��1molCO2����������Ӧ��ֻ�����㰴���ϱ�n��N2����n��CO2��=1��1���뼴�ɣ�
A����0.5molC��2mol NOת��Ϊ��Чƽ��Ϊ0.5molN2��0.5molCO2��1molNO��ʼ�������㣬��A��ѡ��
B.2mol N2��2mol CO2����n��N2����n��CO2��=1��1�����㣬��B��ѡ��
C.1mol C��1mol N2��1mol CO2������C����Ӱ�췴Ӧ��ƽ�ⳣ�����������n��N2����n��CO2��=1��1����C��ѡ��
D.1mol C��1mol NO��1mol N2��ת��Ϊ��Чƽ��Ϊ0.5molC��1.5molN2��0.5molCO2��ʼ�������㣬��D��ѡ��
��ѡBC��
���� ������Ҫ���컯ѧԭ�����֣�����������ԭ��Ӧ����ʽ����д��ƽ�ⳣ���ļ��㣬������ʵĵ���ƽ�⣬��ѧƽ����ƶ���ת���ʵ��жϣ���ѧ��Ӧ���ʵļ��㣬��Чƽ���Ӧ�ã��漰��֪ʶ��϶࣬����ıȽ�ȫ�森�����Ѷ��еȣ�

 �������״���;����㷺��Խ��Խ�����̼ҵĹ�ע����ҵ�ϼ״��ĺϳ�;�����ֶ���������ʵ������ģ��״��ϳɷ�Ӧ����2L�ܱ������ڣ�400��ʱ��Ӧ��CO��g��+2H2��g��?CH3OH��g����H��0����ϵ��n��CO����ʱ��ı仯�����
�������״���;����㷺��Խ��Խ�����̼ҵĹ�ע����ҵ�ϼ״��ĺϳ�;�����ֶ���������ʵ������ģ��״��ϳɷ�Ӧ����2L�ܱ������ڣ�400��ʱ��Ӧ��CO��g��+2H2��g��?CH3OH��g����H��0����ϵ��n��CO����ʱ��ı仯�����| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 5 |
| n��CO����mol�� | 0.020 | 0.011 | 0.008 | 0.007 | 0.007 |
��2����H2��ʾ��0��2s�ڸ÷�Ӧ��ƽ������v��H2��=0.006mol•L-1•s-1��
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����b c��
a��v��CH3OH��=2v��H2�� b��������ѹǿ���ֲ���
c��2v����CO��=v����H2�� d���������ܶȱ��ֲ���
��4����֪���³�ѹ��1gҺ̬�״�ȼ������CO2�����Һ̬ˮ�ų�22.68kJ����������÷�Ӧ���Ȼ�ѧ����ʽΪ��CH3OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+2H2O��l����H=-725.76kJ•mol-1��
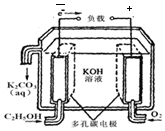
��5��CH3OH��O2�ķ�Ӧ�ɽ���ѧ��ת��Ϊ���ܣ��乤��ԭ����ͼ2��ʾ��ͼ��CH3OH��A����A��B��ͨ�룬b���ĵ缫��Ӧʽ��O2+4e-+2H2O=4OH-��
| A�� | ͬŨ�ȡ�ͬ�����ǿ����ǿ����Һ��Ϻ���Һ�� pH һ������ 7 | |
| B�� | 0.1 mol•L-1 NH4Cl ��Һ�� 0.1 mol•L-1��ˮ�������ϣ�pH��7����c��NH3•H2O����c��NH4+����c��Cl-����c��OH-�� | |
| C�� | �� 0.10 mol•L-1Na2SO3��Һ��ͨ SO2 ��������Һ pH=7��c��Na+���T2c��SO32-��+c��HSO3-�� | |
| D�� | 0.1 mol AgCl �� 0.1 mol AgBr ��Ϻ����ˮ�У�������Һ c��Cl-���Tc��Br-�� |
| A�� | ��Ϊͬλ�ص� 14C��12C | B�� | ��Ϊͬϵ��Ķ������ | ||
| C�� | ��Ϊͬ��������Ľ��ʯ��ʯī | D�� | ��Ϊͬ���칹��ı�ϩ�ͻ����� |