题目内容
碳、氢、氧、氮元素及其化合物与人类的生产生活密切相关,试回答下列有关问题.
(1)常温下0.1mol?L-1NaHCO3 溶液的pH大于8则溶液中c(HCO3-) (填“>”“<”或“=”)c(CO3 2-),原因是
(2)以铝材为阳极,在H2SO4溶液中电解,取少量废电解液,加入NaHCO3 溶液后产生气体和白色沉淀,产生沉淀的原因是 (用离子方程式表示);
(3)用离子方程式表示NaAlO2 溶液的水解 ,写出3种促进AlO2-水解的方法 、 、
(4)关于0.1mol?L-1纯碱溶液,下列四个关系正确的是 .
A.c(Na+ )=2c(CO3 2-) B.c(CO3 2-)>c(OH-)>c(HCO3-)>c(H2CO3)
C.c(CO3 2-)+c(HCO3-)=0.1mol?L-1 D.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
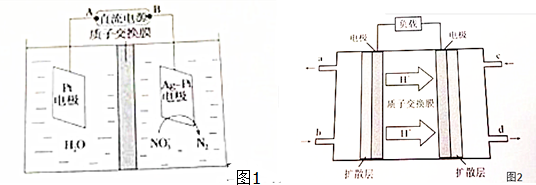
(5)电化学降解NO3-的原理如图1所示阴极反应式为 ,电解后,阴极区pH的将 (填“增大”“减少”或“不变”)
(6)甲醇(CH3OH)~空气燃料电池工作原理示意图如图2:负极的反应式为 .
(1)常温下0.1mol?L-1NaHCO3 溶液的pH大于8则溶液中c(HCO3-)
(2)以铝材为阳极,在H2SO4溶液中电解,取少量废电解液,加入NaHCO3 溶液后产生气体和白色沉淀,产生沉淀的原因是
(3)用离子方程式表示NaAlO2 溶液的水解
(4)关于0.1mol?L-1纯碱溶液,下列四个关系正确的是
A.c(Na+ )=2c(CO3 2-) B.c(CO3 2-)>c(OH-)>c(HCO3-)>c(H2CO3)
C.c(CO3 2-)+c(HCO3-)=0.1mol?L-1 D.c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)
(5)电化学降解NO3-的原理如图1所示阴极反应式为
(6)甲醇(CH3OH)~空气燃料电池工作原理示意图如图2:负极的反应式为

考点:离子浓度大小的比较,化学电源新型电池,盐类水解的应用
专题:
分析:(1)0.1mol?L-1NaHCO3 溶液的pH大于8,溶液显碱性,水解大于其电离;
(2)铝为阳极,失去电子,Al3+和HCO3-发生了互促水解,或HCO3-与H+反应使H+浓度减小,产生Al(OH)3沉淀;
(3)偏铝酸根离子水解显碱性,发生AlO2-+2H2O?Al(OH)3+OH-,结合平衡移动分析;
(4)根据电荷守恒、物料守恒和质子守恒分析;
(5)在电解池的阴极上发生得电子的还原反应;
(6)负极上甲醇失电子发生氧化反应.
(2)铝为阳极,失去电子,Al3+和HCO3-发生了互促水解,或HCO3-与H+反应使H+浓度减小,产生Al(OH)3沉淀;
(3)偏铝酸根离子水解显碱性,发生AlO2-+2H2O?Al(OH)3+OH-,结合平衡移动分析;
(4)根据电荷守恒、物料守恒和质子守恒分析;
(5)在电解池的阴极上发生得电子的还原反应;
(6)负极上甲醇失电子发生氧化反应.
解答:
解:(1)0.1mol?L-1NaHCO3 溶液的pH大于8,溶液显碱性,水解大于其电离,则c(HCO3-)>c(CO3 2-),故答案为:>;HCO3-水解大于其电离;
(2)铝为阳极,会发生氧化反应,生成Al3+,加入NaHCO3溶液后产生气泡和白色沉淀,Al3+和HCO3-发生了互促水解.3HCO3-+Al3+=3CO2↑+Al(OH)3↓;或HCO3-与H+反应使H+浓度减小,产生Al(OH)3沉淀,
故答案为:3HCO3-+Al3+=3CO2↑+Al(OH)3↓;
(3)偏铝酸根离子水解显碱性,发生AlO2-+2H2O?Al(OH)3+OH-,加热、加盐酸、加水等促进AlO2-水解,水解平衡正向移动,故答案为:AlO2-+2H2O?Al(OH)3+OH-;加热;加盐酸;加水;
(4)A.根据物料守恒,碳元素在溶液中的形式有:CO32-、HCO3-、H2CO3、所以c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故A错误;
B.溶液中存在两步水解:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,以第一步水解为主,所以c(CO32-)>c(OH-)>c(HCO3-)>c(H2CO3),故B正确;
C.根据物料守恒:c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol?L-1,故C错误;
D.根据质子守恒:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3),故D正确;
故答案为:BD;
(5)根据装置图示可以看出,右端电极上发生得电子的还原反应,即为阴极,反应式为2NO3-+12H++10e-=N2↑+6H2O,氢离子浓度减小,则pH增大,
故答案为:2NO3-+12H++10e-=N2↑+6H2O;增大;
(6)负极上甲醇失电子和水反应生成二氧化碳和氢离子,电极反应式为2CH3OH-12e-+2H2O=2CO2↑+12H+,故答案为:2CH3OH-12e-+2H2O=2CO2↑+12H+.
(2)铝为阳极,会发生氧化反应,生成Al3+,加入NaHCO3溶液后产生气泡和白色沉淀,Al3+和HCO3-发生了互促水解.3HCO3-+Al3+=3CO2↑+Al(OH)3↓;或HCO3-与H+反应使H+浓度减小,产生Al(OH)3沉淀,
故答案为:3HCO3-+Al3+=3CO2↑+Al(OH)3↓;
(3)偏铝酸根离子水解显碱性,发生AlO2-+2H2O?Al(OH)3+OH-,加热、加盐酸、加水等促进AlO2-水解,水解平衡正向移动,故答案为:AlO2-+2H2O?Al(OH)3+OH-;加热;加盐酸;加水;
(4)A.根据物料守恒,碳元素在溶液中的形式有:CO32-、HCO3-、H2CO3、所以c(Na+)=2c(CO32-)+2c(HCO3-)+2c(H2CO3),故A错误;
B.溶液中存在两步水解:CO32-+H2O?HCO3-+OH-,HCO3-+H2O?H2CO3+OH-,以第一步水解为主,所以c(CO32-)>c(OH-)>c(HCO3-)>c(H2CO3),故B正确;
C.根据物料守恒:c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol?L-1,故C错误;
D.根据质子守恒:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3),故D正确;
故答案为:BD;
(5)根据装置图示可以看出,右端电极上发生得电子的还原反应,即为阴极,反应式为2NO3-+12H++10e-=N2↑+6H2O,氢离子浓度减小,则pH增大,
故答案为:2NO3-+12H++10e-=N2↑+6H2O;增大;
(6)负极上甲醇失电子和水反应生成二氧化碳和氢离子,电极反应式为2CH3OH-12e-+2H2O=2CO2↑+12H+,故答案为:2CH3OH-12e-+2H2O=2CO2↑+12H+.
点评:本题考查较综合,涉及离子浓度大小的比较、电化学及盐类水解等,综合性较强,注重高频考点的考查,题目难度中等.

练习册系列答案
相关题目
短周期主族元素A、B、C、D,原子半径依次减小,其中A的单质是一种重要的半导体材料;B的单质常用于自来水消毒;C是金属,其密度是所有金属中最小;D的一种气态氢化物能使湿润的红色石蕊试纸变蓝.则下列说法错误的是( )
| A、D的气态氢化物比A的气态氢化物稳定 |
| B、A的常见氧化物是一种酸性氧化物,能与水反应生成一种弱酸 |
| C、B的最高价氧化物对应的水化物是酸性最强的含氧酸 |
| D、单质C常温下能与水反应生成一种气体 |
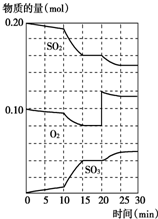 600℃时,在一固定容积的密闭容器中,将二氧化硫和氧气混合发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0.反应过程中SO2、O2、SO3物质的量的变化如图,下列说法错误的是( )
600℃时,在一固定容积的密闭容器中,将二氧化硫和氧气混合发生反应:2SO2(g)+O2(g)?2SO3(g)△H<0.反应过程中SO2、O2、SO3物质的量的变化如图,下列说法错误的是( )| A、反应从开始到第一次平衡时,二氧化硫的转化率为20% |
| B、10~15 min和20~25min相比,前者的化学反应速率大 |
| C、反应进行至20min时,曲线发生变化是因为通入了氧气 |
| D、反应进行到10min~15 min的曲线变化原因一定是增大了压强 |
化学中常借助于图象这一表现手段以清晰地突出实验装置的要点,形象地阐述化学过程的原理.下列有关化学图象表现的内容正确的是( )
A、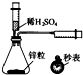 测定一定时间内生成H2的反应速率 |
B、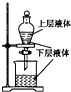 提取海带中的碘 |
C、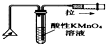 检验火柴燃烧产生的SO2 |
D、 证明非金属性:Cl>C>Si |