题目内容
5.下列说法中正确的是( )| A. | NO2、SO2、BF3、NCl3分子中没有一个分子中原子的最外层电子都满足了8e-稳定结构 | |
| B. | P4和CH4都是正四面体分子且键角都为109°28′ | |
| C. | NaCl晶体中与每个Na+距离相等且最近Na+共有12个 | |
| D. | CsCl晶体中与每个Cs+距离相等且最近Cl-共有6个 |
分析 A.在ABn型化合物中,中心元素A的族序数+成键数=8时,满足分子中所有原子都满足最外层8电子结构;
B.白磷的键角是60°;
C.根据NaCl晶体的晶胞示意图可以看出,与每个Na+距离最近且相等的Cl-共有6个,与每个Na+距离相等且最近Na+共有12个;
D.氯化铯晶体中阴阳离子的配位数是8.
解答 解:A.NCl3中所有原子都达到8电子结构,故A错误;
B.白磷是正四面体结构,但键角是60°,CH4正四面体分子且键角为109°28ˊ,故C错误;
C.根据NaCl晶体的晶胞示意图可以看出,与每个Na+距离最近且相等的Cl-共有6个,与每个Na+距离相等且最近Na+共有12个,故C正确;
D.由氯化铯体的晶胞可知,CsCl晶体中每个Cs+周围紧邻的有8个Cl-,而和每个Cl-等距离紧邻的也有8个Cs+,故D错误;
故选C.
点评 本题考查较综合,涉及8电子稳定结构的判断、键角的判断、晶体的结构等知识点,注意白磷分子中4个磷原子位于四面体4个顶点上,与甲烷的键角不同,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
16.a g铜、铁与一定量浓硝酸反应后,向所得到溶液中加入KSCN溶液无明显变化,将所得其体与1.68L O2(标准状况)混合后通入水中,所有气体能完全被水吸收生成硝酸.则a可能为( )
| A. | 8.4 | B. | 9.6 | C. | 6 | D. | 9.2 |
13.下列物质反应后,固体质量减轻的是( )
| A. | 水蒸气通过灼热的铁粉 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 将Zn片放入CuSO4溶液 | D. | 铝与MnO2发生铝热反应 |
14.用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式2H++SO32-=H2O+SO2↑的反应个数有( )
| A. | 4个 | B. | 6个 | C. | 8个 | D. | 12个 |
15.在氨水中存在NH3•H2O?NH4++OH-的平衡,如果要使平衡向左移动,同时使c(OH-)增大,应加入( )
| A. | NH4Cl固体 | B. | H2SO4 | C. | NaOH固体 | D. | 大量水 |
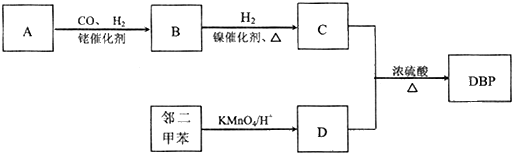
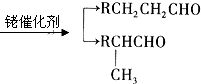
 .
.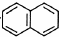 .
.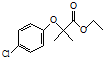 )是临床上一种降脂抗血栓药物,它的一条合成路线如下:
)是临床上一种降脂抗血栓药物,它的一条合成路线如下: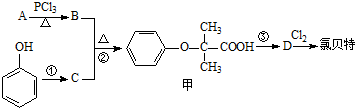
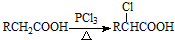
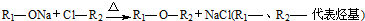
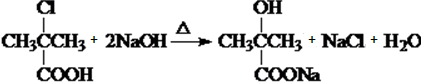 .
.