题目内容
(8分)有二氧化碳与一氧化碳的混合气体共10.8 g,其物质的量为0.3 mol。求:
(1)混合气体中二氧化碳与一氧化碳的物质的量各为多少?
(2)混合气体缓慢通过足量的氢氧化钠溶液后,剩余的气体是什么?其质量为多少?所含分子数为多少?
(1)0.15mol 0.15mol (2)一氧化碳 4.2g 0.15NA=9.03×1022
【解析】
试题分析:(1)设CO、CO2分别为xmol、ymol。则x+y=0.3(C守恒),28x+44y=10.8(质量守恒定律),两式连列解得:x=y=0.15mol,因此CO、CO2的物质的量都为0.15mol。(2)混合气体缓缓通过足量的氢氧化钠后,CO2被NaOH溶液吸收,剩余CO气体,质量为0.15molx28g/mol=4.2g,所含分子数为0.15molxNA=0.15x6.02x1023=9.03x1022
考点:考查物质的量的有关计算。

练习册系列答案
相关题目
 2SO3为放热反应,对该反应的下列说法中正确的是
2SO3为放热反应,对该反应的下列说法中正确的是 Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
 CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.求:
CO2(g)+H2(g),一段时间后该反应达到平衡,测得CO的物质的量为0.5mol.求: 。若误食亚硝酸盐,则导致血红蛋白中
。若误食亚硝酸盐,则导致血红蛋白中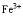 还原为
还原为