题目内容
12.甲同学查阅资料获得,”氨气具有还原性,能还原Cu0”的结论,为证实这一结论的真实性,并验证反应产物,甲同学设计了如下图所示装置进行实验.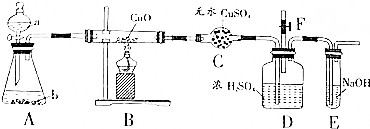
(1)试剂a、b分别是浓氨水、生石灰;
(2)乙同学在研究了甲同学的装置后,发现该装置在设计上有明显缺陷,他对装置进行了改进,改进措施是A、B之间应加入干燥装置;利用改进后的装置进行实验,观察到Cu0变为红色物质,无水CuS04变蓝;打开F导管上的止水夹,向广口瓶中鼓入空气,气体仍为无色,则氨气与氧化铜反应的化学方程式为2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O;
(3)甲同学所设计装置中的E和F导管能更加严密地推断出反应所得产物,你认为E、F的作用分别是通入空气、尾气吸收装置.
分析 如CuO能氧化氨气,可生成NO或N2,实验时,A用于制备氨气,a为浓氨水,b为生石灰,B为反应装置,C用于检验是否生成水,如生成氮气,则通过F通入空气,D中无现象,如生成NO,通过F通入空气,D中无色气体变为红棕色,E为尾气吸收装置,实验时,A、B之间应加入干燥装置,以免为C的实验结果有影响,以此解答该题.
解答 解:如CuO能氧化氨气,可生成NO或N2,实验时,A用于制备氨气,a为浓氨水,b为生石灰,B为反应装置,C用于检验是否生成水,如生成氮气,则通过F通入空气,D中无现象,如生成NO,通过F通入空气,D中无色气体变为红棕色,E为尾气吸收装置,
(1)由以上分析可知a为浓氨水,b为生石灰,生石灰具有吸水作用,且放热,有利于氨气的挥发,故答案为:浓氨水;生石灰;
(2)A、B之间应加入干燥装置,以免为C的实验结果有影响,利用改进后的装置进行实验,观察到Cu0变为红色物质,无水CuS04变蓝,说明生成水,打开F导管上的止水夹,向广口瓶中鼓入空气,气体仍为无色,说明氨气被氧化生成氮气,则氨气与氧化铜反应的化学方程式为2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O,
故答案为:A、B之间应加入干燥装置;2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2+3H2O;
(3)如上分析,如生成NO,通过F通入空气,D中无色气体变为红棕色,E为尾气吸收装置,故答案为:通入空气、尾气吸收装置.
点评 本题考查物质的性质实验的设计,为高考常见题型和高频考点,侧重于学生的分析、实验能力的考查,答题时注意物质的性质以及实验的原理和操作的严密性和合理性的评价,难度不大.

练习册系列答案
相关题目
20.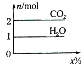 将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )
将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )
 将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )
将甲,乙两种液体混合,取一定质量的该混合液进行完全燃烧实验,生成CO2、H2O的质量与甲气体在混合液中质量分数关系如图所示,甲、乙组合正确的是( )| A | B | C | D | |
| 甲 | 戊烯 | 已烯 | 己二炔(C6H6) | 己烷 |
| 乙 | 环己烷(C6H12) | 苯 | 苯 | 乙醇 |
| A. | A | B. | B | C. | C | D. | D |
7.下列有关化学用语和概念的表达理解正确的是( )
| A. | 立体烷 和苯乙烯 和苯乙烯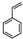 互为同分异构体 互为同分异构体 | |
| B. | 1,3-丁二烯的键线式可表示为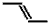 | |
| C. | 二氟化氧分子电子式为  | |
| D. | H216O、D216O、H218O、D218O互为同素异形体 |
17.如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的( )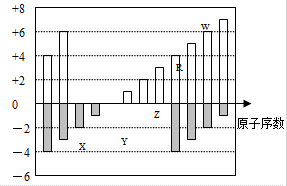

| A. | 单质的氧化性:X>R>W | |
| B. | 气态氢化物的稳定性:R<W | |
| C. | WX2和水反应形成的化合物是一定不能与铜反应 | |
| D. | 离子的氧化性:Z>Y |
4.已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中1mol O=O键完全断裂时吸收热量496kJ,水蒸气中1mol H-O键形成时放出热量463kJ,则氢气中1mol H-H键断裂时吸收热量为( )
| A. | 920kJ | B. | 557kJ | C. | 436kJ | D. | 181kJ |
8.下列说法正确的是( )
| A. | 氢气的燃烧热为△H=-285.5kJ•mol-1,则电解水的热化学方程式为2H2O(l)$\frac{\underline{\;电解\;}}{\;}$2H2(g)+O2(g)△H=+285.5k•Jmol-1 | |
| B. | 反应SO2(g)+2H2S(g)═3S(s)+2H2O(l)在常温下能自发进行,则该反应的△H<0 | |
| C. | 500℃、30MPa下,将0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)═2NH3(g)△H=-38.6k•Jmol-1 | |
| D. | 由C(石墨,s)=C(金刚石,s)△H=+1.90 k•Jmol-1可知,金刚石比石墨稳定 |
9.化学与社会、生活密切相关.下列说法错误的是( )
| A. | 碘酒是指碘单质的乙醇溶液 | |
| B. | 浓硫酸可以刻蚀石英制艺术品 | |
| C. | 84消毒液的有效成分是NaClO | |
| D. | 氢氧化铝、小苏打等可用于治疗胃酸过多 |