题目内容
15.(1)质子数为 8,中子数为 10 的简单氧离子的符号是${{{\;}^{18}}_{8}O}^{2-}$.(2)将等物质的量 Fe2O3与 FeCl3置于密闭管中加热,能恰好完全反应,且只生成一种产物 X,其物质的量是反应物总物质的量的 1.5 倍,写出 X 的化学式FeOCl;
(3)完成以下氧化还原反应的离子方程式:
(2)+MnO4-+5SO32-+6H+=3H2O+2Mn2++5SO42-.
分析 (1)根据质量数=质子数+中子数,计算其质量数为18,依据原子离子符号书写规则书写;
(2)依据反应前后原子守恒分析判断X的化学式;
(3)S:+4→+6,↑2,×5
Mn:+7→+2,↓5,×2
再根据质量守恒定律得出正确结论.
解答 解:(1)根据质量数=质子数+中子数,计算其质量数为18,依据原子离子符号书写规则写出简单氧离子的符号,故答案为:${\;}^{1{8}_{8}}{O}^{2-}$;
(2)将等物质的量Fe2O3与FeCl3置于密闭管中加热,能恰好完全反应,且只生成一种产物X,其物质的量是反应物总物质的量的1.5倍,设Fe2O3与FeCl3物质的量都是1mol,生成X物质的量为3mol,Fe2O3+FeCl3=3X,则依据原子守恒得到:X为FeOCl,
故答案为:FeOCl;
(3)S:+4→+6,↑2,×5
Mn:+7→+2,↓5,×2
故SO32-、SO42-的化学计量数为5,MnO4-、Mn2+的化学计量数为2,由O守恒可知:生成物缺3molH2O,根据电荷守恒守恒可知:反应物中缺6molH+,
故答案为:2,5,6H+,2,5,3H2O.
点评 本题考查了原子符号、离子符号、物质推断、氧化还原方程式的配平方法,原子守恒的分析应用,注意题干条件和信息的理解应用,掌握基础是关键,题目难度中等.

练习册系列答案
 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
5.关于Na2CO3、NaHCO3两种盐的描述错误的是( )
| A. | 可以用加热的方法除去Na2CO3固体中的少量NaHCO3固体 | |
| B. | 可以用澄清石灰水鉴别Na2CO3和NaHCO3两种溶液 | |
| C. | 可以用通CO2气体的方法除去NaHCO3溶液中的Na2CO3 | |
| D. | 饱和Na2CO3溶液中通入CO2气体溶液会出现浑浊 |
6.下列关于置换反应M+X→N+Y其中M、N为单质,X,Y为化合物,反应条件已略去)的说法中正确的是( )
| A. | 若X为氧化物,则Y也一定是氧化物 | |
| B. | 若M为金属单质,则N一定为金属单质 | |
| C. | 若X是不含金属元素的化合物,则N一定是非金属单质 | |
| D. | 若X是含有金属元素的化合物,则Y一定含有金属元素的化合物 |
3.下列有关实验的叙述正确的是( )
| A. | 实验室可用浓硫酸干燥SO2气体 | |
| B. | 准确量取25.00 mL的液体可选用量筒或滴定管等量具 | |
| C. | 无色气体燃烧后生成的气体通入Ba(OH)2溶液,有白色沉淀生成,则原气体一定是CO | |
| D. | FeCl3、CuCl2的混合液中加铁粉充分反应后仍有固体存在,再加KSCN溶液可呈现血红色 |
10.短周期元素 X、Y、Z、W、Q 在周期表中相对位置如图所示,已知 X 元素是地壳中含量最高的元素,下列说法正确的是( )
| X | Y | ||
| Z | W | Q |
| A. | Y 的非金属性比Q强,所以HnY的酸性比HnQ强 | |
| B. | ZX2、WX2的熔沸点、硬度相差很大,这是由于它们的化学键类型不同造成的 | |
| C. | W、Q、Y 元素的原子半径及其简单离子半径依次减小 | |
| D. | 将足量的 X 单质通入 W 的氢化物的水溶液,能得到 W 的低价氧化物 |
20.我国药学家屠呦呦因发现植物黄花蒿叶中含有抗疟疾的物质-青蒿素而荣获2015年诺贝尔奖.科学家对青蒿素的结构进行进一步改良,合成药效更佳的双氢青蒿素、蒿甲醚.下列说法正确的是( )

| A. | 利用黄花蒿叶研究青蒿素结构的基本步骤为:元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式 | |
| B. | ①、②的反应类型分别为还原反应、酯化反应 | |
| C. | 双氢青蒿素在水中的溶解性大于青蒿素 | |
| D. | 双氢青蒿素与蒿甲醚组成上相差-CH2-,二者互为同系物 |
7. H2S利用是回收能量并得到单质硫.反应原理为:2H2S(g)+02(g)=S2(s)+2H20(1)△H=-632kJ•mol-1.图为质子膜H2S燃料电池示意图.下列说法正确的是( )
H2S利用是回收能量并得到单质硫.反应原理为:2H2S(g)+02(g)=S2(s)+2H20(1)△H=-632kJ•mol-1.图为质子膜H2S燃料电池示意图.下列说法正确的是( )
 H2S利用是回收能量并得到单质硫.反应原理为:2H2S(g)+02(g)=S2(s)+2H20(1)△H=-632kJ•mol-1.图为质子膜H2S燃料电池示意图.下列说法正确的是( )
H2S利用是回收能量并得到单质硫.反应原理为:2H2S(g)+02(g)=S2(s)+2H20(1)△H=-632kJ•mol-1.图为质子膜H2S燃料电池示意图.下列说法正确的是( )| A. | 该电池可实现把化学能全部转化为电能 | |
| B. | 电极b上发生的电极反应为:02+2H2O+4e-=40H- | |
| C. | 电极a上发生的电极反应为:2H2S-4e-=S2+4H+ | |
| D. | 标况下,当有22.4LH2S参与反应时,有2mo1H+经质子膜进入负极区 |
4.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=1的溶液中:Na+、NH4+、SO42-、CO32- | |
| B. | 与铝反应产生大量氢气的溶液中:Ca2+、Fe2+、Cl-、NO3- | |
| C. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=10-6的溶液中:K+、Na+、I-,SO42- | |
| D. | c(ClO-)=1.0 mol•L-1的溶液中:Na+、K+、S2-、SO42- |
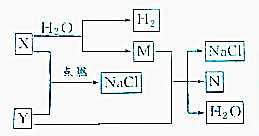 已知下列转化关系:
已知下列转化关系: