题目内容
某化肥厂以氨和空气(其中氧气的体积分数为0.2)为原料生产硝酸铵过程如下: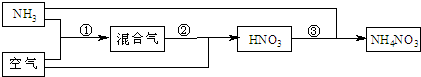
其中反应①为4NH3+5O2
| ||
(1)步骤②中发生了两个反应,将这两个化学方程式合并为一个化学方程式,可表示为
(2)若不考虑副反应且各步反应均完全,为使生产过程中不再补充空气,则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为
(3)假设实际生产中,反应①、②中含氮物质的利用率分别为a、b,反应③中氨的利用率为c、硝酸的利用率为100%,则合成硝酸铵的整个流程中,氨的总利用率是多少?
分析:(1)依据反应②发生的反应2NO+O2 =2NO2和3NO2+H2O=2HNO3+NO,消元即可解答;
(2)依据反应4NH3+5O2
4NO+6H2O①4NO+3O2+2H2O=4HNO3 ②NH3+HNO3=NH4NO3 ③消元即可解答;
(3)根据氮原子守恒和含氮物质的利用率进行解答,假设消耗NH3的总物质的量为1mol,其中用于制取HNO3的NH3的物质的量为x mol,反应①、②中生成的硝酸为abx mol;假设第①步参加反应的氨气的物质的量为4mol,生成硝酸的物质的量4abmol;
(2)依据反应4NH3+5O2
| ||
(3)根据氮原子守恒和含氮物质的利用率进行解答,假设消耗NH3的总物质的量为1mol,其中用于制取HNO3的NH3的物质的量为x mol,反应①、②中生成的硝酸为abx mol;假设第①步参加反应的氨气的物质的量为4mol,生成硝酸的物质的量4abmol;
解答:解:(1)反应②涉及这样几步反应:2NO+O2 =2NO2 A,3NO2+H2O=2HNO3+NO B,A×3+B×2,消去中间物NO2,得:4NO+3O2+2H2O=4HNO3,
故答案为:4NO+3O2+2H2O=4HNO3;
(2)整个过程包括这样几步反应:4NH3+5O2
4NO+6H2O①4NO+3O2+2H2O=4HNO3 ②
NH3+HNO3=NH4NO3 ③,将①+②+③×4,约简得:2NH3+2O2=NH4NO3 +H2O
由n(NH3):n(O2)=1:1 推知V(NH3):V(空气)=1:5 则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为
=
;
故答案为:
(或16.7%);
(3)解法一:假设消耗NH3的总物质的量为1mol,其中用于制取HNO3的NH3的物质的量为x mol,被HNO3吸收的NH3的物质的量为ymol,反应①、②中生成的硝酸为abxmol,NH3+HNO3=NH4NO3 ,abx=cy,则:x+y=1、abx=cy,解得:x=
,y=
,氨的总利用率=
=
;
解法二:假设第①步参加反应的氨气的物质的量为4mol,反应①、②中含氮物质的利用率分别为a、b,则:生成硝酸的物质的量4abmol,NH3+HNO3=NH4NO3 ,反应③中氨的利用率为c,第③步需要氨气的物质的量为
mol;
氨的总利用率=
=
;
故答案为:
;
故答案为:4NO+3O2+2H2O=4HNO3;
(2)整个过程包括这样几步反应:4NH3+5O2
| ||
NH3+HNO3=NH4NO3 ③,将①+②+③×4,约简得:2NH3+2O2=NH4NO3 +H2O
由n(NH3):n(O2)=1:1 推知V(NH3):V(空气)=1:5 则原料气中氨(包括第③步被硝酸吸收的氨)的体积分数最大值为
| 1 |
| 1+5 |
| 1 |
| 6 |
故答案为:
| 1 |
| 6 |
(3)解法一:假设消耗NH3的总物质的量为1mol,其中用于制取HNO3的NH3的物质的量为x mol,被HNO3吸收的NH3的物质的量为ymol,反应①、②中生成的硝酸为abxmol,NH3+HNO3=NH4NO3 ,abx=cy,则:x+y=1、abx=cy,解得:x=
| c |
| ab+c |
| ab |
| ab+c |
| xab+yc |
| 1 |
| 2abc |
| ab+c |
解法二:假设第①步参加反应的氨气的物质的量为4mol,反应①、②中含氮物质的利用率分别为a、b,则:生成硝酸的物质的量4abmol,NH3+HNO3=NH4NO3 ,反应③中氨的利用率为c,第③步需要氨气的物质的量为
| 4ab |
| c |
氨的总利用率=
| 4ab+4ab | ||
4+
|
| 2abc |
| ab+c |
故答案为:
| 2abc |
| ab+c |
点评:本题考查了以硝酸的工业制备流程背景下的化学计算,关键是依据各生产原料和产物间的关系,将方程式当作代数式进行相应的消元,构建目标物质的关系,题目难度中等.

练习册系列答案
相关题目


