题目内容
工业上有一反应2A(g)+B(g)![]() 3C(g),按体积比为A∶B=5∶2将A和B充入到一定容积的密闭容器中,若在恒温条件下达到平衡时C占总体积的60%,设A,B,C的相对分子质量分别用a,b,c表示。试求:
3C(g),按体积比为A∶B=5∶2将A和B充入到一定容积的密闭容器中,若在恒温条件下达到平衡时C占总体积的60%,设A,B,C的相对分子质量分别用a,b,c表示。试求:
(1)平衡时A和B的转化率。
(2)平衡时混合气体的平均分子量。
(1)平衡时A的转化率为56%;B的转化率70%;
(2)平衡时混合气体的平均分子量为(5a+2b)/7。
解析:
(1)设A=5V,则B=2V。
设B转化了x,则有:
2A(g)+B(g)![]() 3C(g)
3C(g)
起始 5V 2V? 0
转化 2x x 3x?
平衡 5V-2x 2V-x 3x
依题意有:
(3x)/[(5V-2x)+(2V-x)+3x]
??=(60/100)=(3/5)
即有:(3x/7V)=(3/5)
解得:x=(7V/5)
∴A的转化率为:
A%=(2x/5V)×100%=(2×7/5V)/5V×100%
?=56%
B的转化率为
B%=(x/2V)×100%=(7/5V)/2V×100%=70%
(2)混合气体平衡时的总体积V总=7L
![]() =(5aL+2bL)/7L=(5a+2b)/7
=(5aL+2bL)/7L=(5a+2b)/7

 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案以下是一些元素的信息,其中有一种元素不在短周期。根据信息完成问题:
| 元素A | 元素B | 元素C | 元素X | 元素Y | 元素Z |
| 单质是一种常见金属,与元素X形成黑色和砖红色两种化合物 | 单质是一种黄绿色气体 | 短周期中金属性最强,与X反应能生成两种化合物 | 最外层电子数是内层电子数的3倍,能形成双原子阴离子 | 单质为双原子分子,结构中 | 阳离子就是一个质子 |
(1)写出A元素基态原子的核外电子排布式 。
(2)B、C、X的简单离子半径由大到小的顺序为 (用元素离子符号表示)。
(3)化合物YZ4B化学键的类型是 ,检验该固体化合 物中阳离子的实验的方法和现象是 。
(4)A元素的单质在潮湿空气中锈蚀生成绿色物质,用一个化学方程式表示锈蚀过程 。
(5)常温下,工业上用惰性电极在电解槽中电解100 L 1.5mol·L-1CB的水溶液时,两极共收集到气体22.4L(标准状况下),计算电解后阴极区溶液的pH= (假设电解前后溶液体积不变)。
以下是一些元素的信息,其中有一种元素不在短周期。根据信息完成问题:
| 元素A | 元素B | 元素C | 元素X | 元素Y | 元素Z |
| 单质是一种常见金属,与元素X形成黑色和砖红色两种化合物 | 单质是一种黄绿色气体 | 短周期中金属性最强,与X反应能生成两种化合物 | 最外层电子数是内层电子数的3倍,能形成双原子阴离子 | 单质为双原子分子,结构中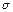 键与 键与 键数目比为1:2 键数目比为1:2 | 阳离子就是一个质子 |
(2)B、C、X的简单离子半径由大到小的顺序为 (用元素离子符号表示)。
(3)化合物YZ4B化学键的类型是 ,检验该固体化合 物中阳离子的实验的方法和现象是 。
(4)A元素的单质在潮湿空气中锈蚀生成绿色物质,用一个化学方程式表示锈蚀过程 。
(5)常温下,工业上用惰性电极在电解槽中电解100 L 1.5mol·L-1CB的水溶液时,两极共收集到气体22.4L(标准状况下),计算电解后阴极区溶液的pH= (假设电解前后溶液体积不变)。