题目内容
19.H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了甲、乙两种实验装置.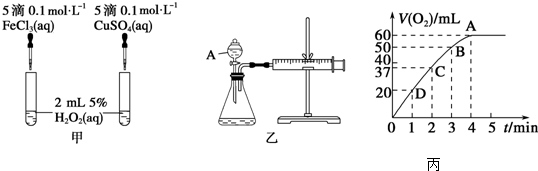
(1)若利用甲实验,可通过观察产生气泡的快慢现象,从而定性比较得出结论.有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是消除阴离子不同对实验的干扰,写出H2O2在二氧化锰催化作用下发生反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,若利用乙实验可进行定量分析,图中仪器A的名称为分液漏斗,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是产生40mL气体所需的时间.
(2)将0.1mol MnO2粉末加入50mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图丙所示,解释反应速率变化的原因:随着反应的进行,浓度减小,反应速率减慢,H2O2初始物质的量浓度为0.11 mol/L(保留两位有效数字).
(3)为了加深同学们对影响反应速率因素的认识,老师让同学完成如下实验:在上述实验装置的锥形瓶内加入6.5g锌粒,通过分液漏斗加入40mL 2.5mol•L-1的硫酸,10s时收集产生的H2的体积为44.8mL(标准状况),用硫酸表示10s内该反应的速率为0.005 mol•L-1•s-1(假设反应前后溶液的体积不变).
分析 (1)比较反应速率的大小可通过生成气泡的快慢来判断,比较金属阳离子的催化效果要排斥阴离子的干扰;H2O2在二氧化锰催化作用下分解产生水和氧气;A仪器名称是分液漏斗;根据v=△c/△t分析实验中还需要测量的数据是时间;
(2)随着反应的进行,溶液的浓度逐渐降低,反应速率逐渐减小;根据图象可以看出H2O2完全反应放出60 mL O2,根据2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑进行计算;
(3)根据Zn+H2SO4=ZnSO4+H2↑,v=△c/△t进行计算.
解答 解:(1)该反应中产生气体,可根据生成气泡的快慢判断,氯化铁和硫酸铜中阴阳离子都不同,无法判断是阴离子起作用还是阳离子起作用,硫酸铁和硫酸铜阴离子相同,可以消除阴离子不同对实验的干扰,在二氧化锰作催化剂条件下,双氧水分解生成水和氧气,反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,A仪器名称是分液漏斗;根据v=△c/△t知,还需要测定产生40mL气体所需的时间,
故答案为:产生气泡的快慢;消除阴离子不同对实验的干扰;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;分液漏斗;产生40mL气体所需的时间;
(2)在二氧化锰作催化剂条件下,双氧水分解生成水和氧气,反应方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,浓度越大,反应速率越大,反之越小,随着反应进行,反应物的浓度逐渐减小,则速率逐渐减小;根据图象可以看出H2O2完全反应放出60 mL O2,H2O2的分解反应为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,则n(H2O2)=$\frac{0.06L}{22.4L/mol}$×2≈0.00536 mol,c(H2O2)=$\frac{0.00536mol}{0.05L}$≈0.11 mol/L,
故答案为:随着反应的进行,浓度减小,反应速率减慢;0.11 mol/L;
(3)Zn+H2SO4=ZnSO4+H2↑
1mol 22.4L
0.002mol 0.0448L
用硫酸表示10s内该反应的速率为v=$\frac{0.002mol}{0.04L×10s}$=0.005mol•L-1•s-1,
故答案为:0.005.
点评 本题考查实验方案设计,根据v=△c/△t来设计实验,通过得到气体的体积和时间的关系确定影响反应速率的因素,难度中等.

 阅读快车系列答案
阅读快车系列答案(1)c(H+)═c(OH-)=10-6mol/L的溶液一定呈中性
(2)已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.3kJ•mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出57.3kJ的热量
(3)向淀粉溶液中加入稀H2SO4,加热几分钟,冷却后再加入新制Cu(OH)2悬浊液,加热,无砖红色沉淀生成,说明淀粉没有水解生成葡萄糖
(4)同一主族的元素,原子半径越大,其单质的熔点不一定越高
(5)乙酸乙酯在NaOH溶液(H218O)中水解产物为CH3CO18ONa和CH3CH2OH
(6)水的电子式 H+[:O:]2-H+.
| A. | (1)(2)(5)(6) | B. | (1)(4)(5) | C. | (2)(4)(6) | D. | 全部 |
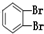
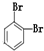
| A. | CH3CH2CHBrCH2Br | B. | CH3CHBrCHBrCH3 | C. | 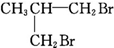 | D. | 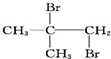 |
(1)下列描述错误的是acde.
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种.现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解.
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色.据此可以推断:该溶液肯定存在的离子是:CO32-、Br-、Na+、SO32-
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验.将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间.
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol•L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
V1=30,V6=10,V9=17.5;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降.请分析氢气生成速率下降的主要原因:当加入一定量的CuSO4后,生成的单质Cu会沉积在Zn的表面,降低了Zn与H2SO4溶液的接触面积而使反应速率下降.
| A. | 溴苯中混有溴,加入KI溶液,振荡,用直馏汽油萃取,分液 | |
| B. | 硝基苯中混有浓硝酸,加入足量稀NaOH溶液洗涤,振荡,用分液漏斗分液 | |
| C. | 乙烯中含有SO2,将其通入装有KMnO4溶液的洗气瓶中进行洗气 | |
| D. | 乙烷中含有乙烯,通入适量的H2在一定条件下反应使乙烯转变成乙烷 |
| A. | C3H7Cl | B. | C3H6 | C. | CF2Cl2 | D. | C4H6 |
 ⑪
⑪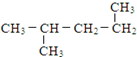 ⑫
⑫