题目内容
由相同条件下的三个反应:①2NaA+B2=2NaB+A2; ②2NaC+A2=2NaA+C2;③2NaB+D2=2NaD+B2;可判断( )
| A、氧化性:A2>B2>C2>D2 |
| B、还原性:C->A->B->D- |
| C、2NaD+A2=2NaA+D2可进行 |
| D、2NaC+B2=2NaB+C2不能进行 |
考点:氧化性、还原性强弱的比较,氧化还原反应
专题:
分析:同一化学反应中氧化剂的氧化性大于氧化产物的氧化性,还原剂的还原性大于还原产物的还原性,据此分析解答.
解答:
解:A、2NaA+B2=2NaB+A2中氧化性B2大于A2,2NaC+A2=2NaA+C2中氧化性A2大于C2,2NaB+D2=2NaD+B2中氧化性D2大于B2,所以氧化性大小顺序为:D2>B2>A2>C2,故A错误.
B、2NaA+B2=2NaB+A2中还原性A-大于B-,2NaC+A2=2NaA+C2中还原性C->A-,2NaB+D2=2NaD+B2中还原性B->D-,所以还原性大小顺序为:C->A->B->D-,故B正确.
C、2NaD+A2=2NaA+D2反应中D2的氧化性大于A2,不符合A得到的结论,不可以进行,故C错误.
D、2NaC+B2=2NaB+C2反应中B2的氧化性大于C2,符合A得到的结论,所以可以进行,故D错误.
故选B.
B、2NaA+B2=2NaB+A2中还原性A-大于B-,2NaC+A2=2NaA+C2中还原性C->A-,2NaB+D2=2NaD+B2中还原性B->D-,所以还原性大小顺序为:C->A->B->D-,故B正确.
C、2NaD+A2=2NaA+D2反应中D2的氧化性大于A2,不符合A得到的结论,不可以进行,故C错误.
D、2NaC+B2=2NaB+C2反应中B2的氧化性大于C2,符合A得到的结论,所以可以进行,故D错误.
故选B.
点评:本题考查了氧化性强弱比较和还原性强弱比较,以及利用强弱关系判断离子方程式正误,题目比较基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,5.6L氯气和16.8L氧气的混合气体中含有分子数为NA |
| B、标准状况下,22.4LH2O所含有原子数为3NA |
| C、NA个N2分子所占的体积与0.5 NA个H2分子所占的体积比一定是2:1 |
| D、常温下,2.3g Na完全与O2反应失去的电子数为0.2NA |
在3Cu2S+22HNO3=6Cu(NO3)2+10NO↑+3H2SO4+8H2O的反应中,转移电子的总数为( )
| A、12 | B、22 | C、24 | D、30 |
1.5mol空气在标准状况下占有的体积是( )
| A、22.4L |
| B、33.6L |
| C、44.8L |
| D、67.2L |
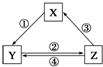 下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )
下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )