题目内容
 【化学--选修2化学与技术】
【化学--选修2化学与技术】黄铁矿是我国大多数硫酸厂制取硫酸的主要原料.某化学兴趣小组对某黄铁矿石(主要 成分为FeS2)进行硫元素含量测定的实验探究及工业生产硫酸的探究.
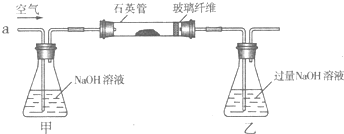
Ⅰ.将m1g该黄铁矿样品(杂质中不含硫和铁)放入如图所示装置(夹持和加热装置 省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全.石英管中发生反应的化学方程式为:4FeS2+11O2
| ||
Ⅱ.反应结束后,将乙瓶中的溶液进行如下处理:

(1)Ⅰ中,乙瓶内发生反应的离子方程式有
(2)Ⅱ中,所加H2O2溶液需足量的理由是
(3)该黄铁矿石中硫元素的质量分数为
(4)简述在催化反应室中设置热交换器的目的:
(5)工业生产中常用氨--硫酸法进行尾气脱硫,以达到消除污染、废物利用的目的,用 两个化学方程式表示其反应原理
考点:探究物质的组成或测量物质的含量
专题:实验探究和数据处理题
分析:(1)甲瓶是利用氢氧化钠溶液吸收空气中的二氧化碳,避免干扰乙装置对二氧化硫的定量测定;乙瓶内是二氧化硫和氢氧化钠反应生成亚硫酸钠,亚硫酸钠被氧气氧化为硫酸钠;
(2)过氧化氢可以把乙瓶中的亚硫酸钠氧化为硫酸钠;
(3)依据硫元素守恒计算分析得到;
(4)依据反应原理和反应过程中催化氧化的目的是氧化二氧化硫为三氧化硫,反应是放热反应,热交换器可以利用放出的热量预热参加反应的二氧化硫和氧气;
(5)二氧化硫和氨气水反应生成亚硫酸铵或亚硫酸氢铵,亚硫酸铵或亚硫酸氢铵和硫酸反应生成硫酸铵,二氧化硫和水.
(2)过氧化氢可以把乙瓶中的亚硫酸钠氧化为硫酸钠;
(3)依据硫元素守恒计算分析得到;
(4)依据反应原理和反应过程中催化氧化的目的是氧化二氧化硫为三氧化硫,反应是放热反应,热交换器可以利用放出的热量预热参加反应的二氧化硫和氧气;
(5)二氧化硫和氨气水反应生成亚硫酸铵或亚硫酸氢铵,亚硫酸铵或亚硫酸氢铵和硫酸反应生成硫酸铵,二氧化硫和水.
解答:
解:(1)甲瓶是利用氢氧化钠溶液吸收空气中的二氧化碳,提供氧气氧化硫铁矿,避免二氧化碳干扰乙装置对二氧化硫的定量测定;乙瓶内是二氧化硫和氢氧化钠反应生成亚硫酸钠,亚硫酸钠被氧气氧化为硫酸钠,反应的离子方程式为SO2+2OH-=SO32-+H2O、2SO32-+O2=2SO42-,
故答案为:SO2+2OH-=SO32-+H2O;2SO32-+O2=2SO42-;
(2)由流程可知加入过氧化氢把亚硫酸钠氧化为硫酸钠,且不引入杂质,故答案为:使SO32-完全氧化为SO42-;
(3)将m1 g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全,生成的二氧化硫被过量氢氧化钠吸收生成亚硫酸钠,部分被氧化为硫酸钠,加入过氧化氢把亚硫酸钠全部氧化为硫酸钠,加入过量绿化比溶液得到沉淀质量为m2g为硫酸钡的质量,物质的量=
mol;
则黄铁矿中硫元素的质量分数=
×100%=
×100%,
故答案为:
×100%;
(4)依据反应原理和反应过程中催化氧化的目的是氧化二氧化硫为三氧化硫,反应是放热反应,热交换器可以利用放出的热量预热参加反应的二氧化硫和氧气,
故答案为:利用二氧化硫被氧化为三氧化硫时放出的热量来预热即将参加反应的二氧化硫和氧气;
(5)二氧化硫和氨气水反应生成亚硫酸铵或亚硫酸氢铵,亚硫酸铵或亚硫酸氢铵和硫酸反应生成硫酸铵,二氧化硫和水,反应的化学方程式为:SO2+NH3+H2O=NH4HSO3或SO2+2NH3+H2O=(NH4)2SO4,2NH4HSO3+H2SO4=(NH4)2SO4+2SO2↑+2H2O或(NH4)2SO3+H2SO4=(NH4)2SO4+SO2↑+H2O,
故答案为:SO2+NH3+H2O=NH4HSO3或SO2+2NH3+H2O=(NH4)2SO4;2NH4HSO3+H2SO4=(NH4)2SO4+2SO2↑+2H2O或(NH4)2SO3+H2SO4=(NH4)2SO4+SO2↑+H2O.
故答案为:SO2+2OH-=SO32-+H2O;2SO32-+O2=2SO42-;
(2)由流程可知加入过氧化氢把亚硫酸钠氧化为硫酸钠,且不引入杂质,故答案为:使SO32-完全氧化为SO42-;
(3)将m1 g该黄铁矿样品放入如图1所示装置(夹持和加热装置省略)的石英管中,从a处不断地缓缓通入空气,高温灼烧石英管中的黄铁矿样品至反应完全,生成的二氧化硫被过量氢氧化钠吸收生成亚硫酸钠,部分被氧化为硫酸钠,加入过氧化氢把亚硫酸钠全部氧化为硫酸钠,加入过量绿化比溶液得到沉淀质量为m2g为硫酸钡的质量,物质的量=
| m2 |
| 233 |
则黄铁矿中硫元素的质量分数=
| ||
| m1 |
| 32m2 |
| 233m1 |
故答案为:
| 32m2 |
| 233m1 |
(4)依据反应原理和反应过程中催化氧化的目的是氧化二氧化硫为三氧化硫,反应是放热反应,热交换器可以利用放出的热量预热参加反应的二氧化硫和氧气,
故答案为:利用二氧化硫被氧化为三氧化硫时放出的热量来预热即将参加反应的二氧化硫和氧气;
(5)二氧化硫和氨气水反应生成亚硫酸铵或亚硫酸氢铵,亚硫酸铵或亚硫酸氢铵和硫酸反应生成硫酸铵,二氧化硫和水,反应的化学方程式为:SO2+NH3+H2O=NH4HSO3或SO2+2NH3+H2O=(NH4)2SO4,2NH4HSO3+H2SO4=(NH4)2SO4+2SO2↑+2H2O或(NH4)2SO3+H2SO4=(NH4)2SO4+SO2↑+H2O,
故答案为:SO2+NH3+H2O=NH4HSO3或SO2+2NH3+H2O=(NH4)2SO4;2NH4HSO3+H2SO4=(NH4)2SO4+2SO2↑+2H2O或(NH4)2SO3+H2SO4=(NH4)2SO4+SO2↑+H2O.
点评:本题考查了物质性质的实验验证和流程分析判断,物质性质和干信息的利用是解题关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
把0.02mol/L CH3COOH溶液和0.01mol/L NaOH溶液以等体积混和后溶液显酸性,则混合液中微粒浓度关系正确的为( )
| A、c(CH3COO-)<c(Na+) |
| B、c(CH3COOH)+c(CH3COO-)=0.02mol/L |
| C、c(CH3COOH)>c(CH3COO-) |
| D、c(OH-)+c(CH3COO-)═c(H+)+c(Na+) |
关于电解槽的叙述中不正确的是( )
| A、与电源正极相连接的是电解槽的阳极 |
| B、与电源负极相连接的是电解槽的阴极 |
| C、电流从电源的负极沿导线流人电解槽的阴极 |
| D、在电解槽的阳极发生氧化反应 |
某国外化学教材中有一张关于氧化还原反应的插图:由图可知, 在该反应中是( )
在该反应中是( )
 在该反应中是( )
在该反应中是( )
| A、还原剂 | B、氧化剂 |
| C、氧化产物 | D、还原产物 |
下列实验能够达到预期目的是( )
| A、在一支盛有2mL 2% CuSO4溶液的试管中,滴入几滴10%的NaOH溶液,再加入1mL乙醛溶液,加热后可以看到红色氧化亚铜沉淀生成 |
| B、将乙酸乙酯与NaOH溶液混合并用水浴加热,即可得到水解产物乙醇和乙酸 |
| C、检验淀粉已经水解,将淀粉与少量稀硫酸加热一段时间后,加入NaOH溶液中和硫酸,再加入银氨溶液加热 |
| D、在一支试管中滴入10滴溴乙烷,再加入1mL 5%的NaOH溶液,共热后滴加硝酸银溶液,可观察到有浅黄色溴化银沉淀生成 |