题目内容
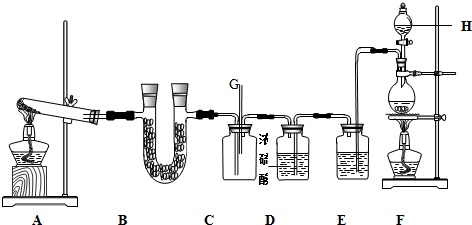
5.烃A是一种植物生长的调节剂,分子式为C2H4,A进行下图1所示的转化可制得有果香味的液体E(C4H8O2),回答下列问题:
(1)A的结构简式为CH2=CH2,B中所含官能团的名称为羟基.
(2)①④反应的类型分别是加成反应、取代反应.
(3)反应②的化学方程式为2 CH3CH2OH+O2$→_{△}^{Cu}$2 CH3CHO+2 H2O.
(4)E的名称为乙酸乙酯.实验室由反应④制备E的装置如图2,烧杯中加入碎瓷片的作用是防止暴沸,长导管的作用是导气和冷凝、回流,锥形瓶中盛放的液体是饱和Na2CO3溶液.
分析 A是一种植物生长的调节剂,分子式为C2H4,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,乙醛进一步氧化生成D为CH3COOH,乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3,以此解答该题.
解答 解:A是一种植物生长的调节剂,分子式为C2H4,则A为CH2=CH2,乙烯与水发生加成反应生成B为CH3CH2OH,乙醇发生催化氧化生成C为CH3CHO,乙醛进一步氧化生成D为CH3COOH,乙酸与乙醇发生酯化反应生成E为CH3COOCH2CH3.
(1)A的结构简式为CH2=CH2,B为CH3CH2OH,所含官能团为:羟基,故答案为:CH2=CH2;羟基;
(2)反应①为加成反应,反应④为取代反应,故答案为:加成反应;取代反应;
(3)反应②的化学方程式为:2 CH3CH2OH+O2$→_{△}^{Cu}$2 CH3CHO+2 H2O,
故答案为:2 CH3CH2OH+O2$→_{△}^{Cu}$2 CH3CHO+2 H2O;
(4)E的名称为:乙酸乙酯.实验室由反应④制备E的装置如图2烧瓶中加入碎瓷片的作用是:防止暴沸,长导管的作用是导气和冷凝、回流,锥形瓶中盛放的液体是饱和Na2CO3溶液,
故答案为:乙酸乙酯;防止暴沸;冷凝、回流;饱和Na2CO3溶液.
点评 本题考查有机物的推断,为高频考点,侧重于学生的分析能力的考查,题目比较基础,涉及酯、醇、醛、羧酸性质,注意对基础知识的理解掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列有机物中,能在铜的作用下催化氧化又能发生消去反应,且消去生成物中存在同分异构体的是( )
| A. | CH3CH2C(OH)(CH3)2 | B. | (CH3)2 CHOH | C. | CH3CH(OH)CH2CH3 | D. | 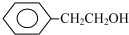 |
16.湿润的淀粉碘化钾试纸接触某气体而显蓝色,该气体可能是①Cl2②NO2③H2S④SO2⑤溴蒸气⑥HCl中的
( )
( )
| A. | ①④⑤ | B. | ①②⑤ | C. | ①②⑥ | D. | ①②④⑤ |
20.现有一装置如图所示(G表示电流计),下列有关说法不正确的是( )
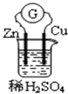

| A. | 该装置将化学能转化为电能 | B. | Zn是负极,发生还原反应 | ||
| C. | 电子由锌片通过导线流向铜片 | D. | 铜片上发生的反应为 2H++2e-═H2↑ |
10.乙醇和二甲醚互为同分异构体,下列说法不正确的是( )
| A. | 乙醇和二甲醚的分子式相同,结构不同 | |
| B. | 乙醇和二甲醚的物理性质不同,化学性质相同 | |
| C. | 二者完全燃烧后的产物相同 | |
| D. | 1mol二甲醚分子中含有8NA共价键 |
14.I.在实验室利用如图装置,可制备某些气体并验证其化学性质.

完成下列表格:
II.工业上用乙烯、氯化氢和氯气为原料,经下列各步合成聚氯乙烯(PVC):
乙烯$→_{①}^{一定条件}$A$→_{②}^{NaOH/乙醇}$B$→_{③}^{一定条件}$C$→_{④}^{一定条件}$PVC
A的结构简式是CH2ClCH2Cl;
反应④的化学方程式是 .
.

完成下列表格:
| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
| (1) | 乙烯 | B→D→E | CH3-CH2-OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O |
| (2) | 乙炔 | A→C→E | CaC2+2H2O→Ca(OH)2+C2H2↑ |
乙烯$→_{①}^{一定条件}$A$→_{②}^{NaOH/乙醇}$B$→_{③}^{一定条件}$C$→_{④}^{一定条件}$PVC
A的结构简式是CH2ClCH2Cl;
反应④的化学方程式是
 .
.
15.为了探究化学反应速率和化学反应限度的有关问题,某研究小组进行了以下实验:
Ⅰ.以H2O2的分解反应为研究对象,实验方案与数据记录如表,t表示收集a mL O2所需的时间:
(1)设计实验2和实验3的目的是研究H2O2的浓度对化学反应速率的影响;
(2)为研究温度对化学反应速率的影响,可以将实验2和实验4作对比(填序号);
(3)将实验1和实验2作对比,t1>t2(填“>”、“<”或“=”).
Ⅱ.以KI和FeCl3反应为例(2Fe3++2I-?2Fe2++I2)设计实验,探究此反应存在一定的限度.可选试剂:
①0.1mol•L-1KI溶液②0.1mol•L-1 FeCl3溶液③0.1mol•L-1 FeCl2溶液
④0.1mol•L-1盐酸⑤0.1mol•L-1KSCN溶液⑥CCl4
实验步骤:
(1)取5mL 0.1mol•L-1 KI溶液,再滴加几滴0.1mol•L-1 FeCl3溶液;
(2)充分反应后,将溶液分成三份;
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘;
(4)另取一份,加试剂⑤(填序号),溶液出现血红色现象,说明此反应存在一定的限度.
Ⅲ.N2O4可分解为NO2.在100mL密闭容器中投入0.01mol N2O4,利用现代化学实验技术跟踪测量c(NO2).c(NO2)随时间变化的数据记录如图所示:
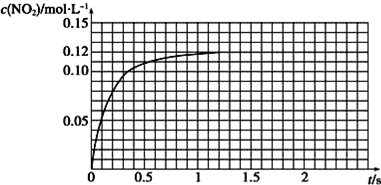
(1)反应容器中最后剩余的物质有NO2、N2O4,其中N2O4的物质的量为0.004molmol;
(2)c(NO2)随时间变化的曲线表明,实验测得的化学反应速率在逐渐减小,最后不变.(选填“变大”,“变小”或“不变”)
Ⅰ.以H2O2的分解反应为研究对象,实验方案与数据记录如表,t表示收集a mL O2所需的时间:
| 序号 | 反应 温度/℃ | c(H2O2)/ mol•L-1 | V(H2O2) /mL | m(MnO2) /g | t/min |
| 1 | 20 | 2 | 10 | 0 | t1 |
| 2 | 20 | 2 | 10 | 0.1 | t2 |
| 3 | 20 | 4 | 10 | 0.1 | t3 |
| 4 | 40 | 2 | 10 | 0.1 | t4 |
(2)为研究温度对化学反应速率的影响,可以将实验2和实验4作对比(填序号);
(3)将实验1和实验2作对比,t1>t2(填“>”、“<”或“=”).
Ⅱ.以KI和FeCl3反应为例(2Fe3++2I-?2Fe2++I2)设计实验,探究此反应存在一定的限度.可选试剂:
①0.1mol•L-1KI溶液②0.1mol•L-1 FeCl3溶液③0.1mol•L-1 FeCl2溶液
④0.1mol•L-1盐酸⑤0.1mol•L-1KSCN溶液⑥CCl4
实验步骤:
(1)取5mL 0.1mol•L-1 KI溶液,再滴加几滴0.1mol•L-1 FeCl3溶液;
(2)充分反应后,将溶液分成三份;
(3)取其中一份,加试剂⑥,振荡,CCl4层显紫色,说明反应生成碘;
(4)另取一份,加试剂⑤(填序号),溶液出现血红色现象,说明此反应存在一定的限度.
Ⅲ.N2O4可分解为NO2.在100mL密闭容器中投入0.01mol N2O4,利用现代化学实验技术跟踪测量c(NO2).c(NO2)随时间变化的数据记录如图所示:

(1)反应容器中最后剩余的物质有NO2、N2O4,其中N2O4的物质的量为0.004molmol;
(2)c(NO2)随时间变化的曲线表明,实验测得的化学反应速率在逐渐减小,最后不变.(选填“变大”,“变小”或“不变”)
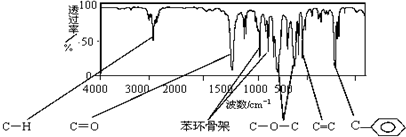
 .
.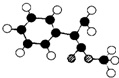 (图中球与球之间连线表示单键或双键).
(图中球与球之间连线表示单键或双键).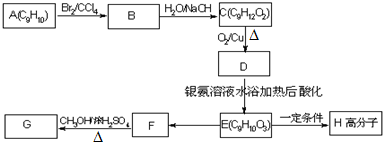
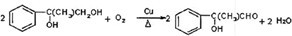 .E→H
.E→H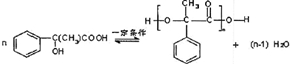 .
.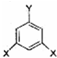 (其中X、Y均不为H),试写出符合上述通式且能发生银镜反应和遇氯化铁溶液发生显色反应的2种物质的结构简式
(其中X、Y均不为H),试写出符合上述通式且能发生银镜反应和遇氯化铁溶液发生显色反应的2种物质的结构简式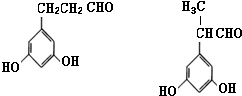 .
.