题目内容
孔雀石主要含Cu2(OH)2CO3,还含少量Fe的氧化物和SiO2,实验室以孔雀石为原料制备CuSO4?5H2O及CaCO3,步骤如图1:
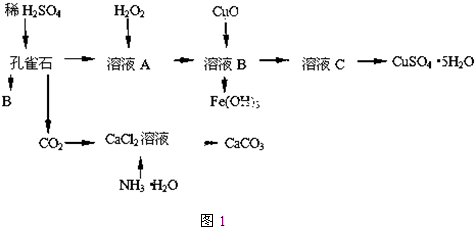
试回答下列问题:
(1)B物质的化学式是 在未加入H2O2的溶液中,存在的金属离子有Cu2+、Fe2+、Fe3+.若检验该溶液中Fe3+,选择最合适的试剂是 (填代号).
A.KMnO4溶液 B.Fe粉 C. Na2CO3溶液 D. KSCN溶液
(2)向溶液A加入H2O2的作用是 剂(填氧化或还原),离子反应方程式为 ,选用H2O2而不用Cl2的原因是 .
(3)由溶液C获得CuSO4?5H2O,需要经过 ,过滤等操作.除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器是 .
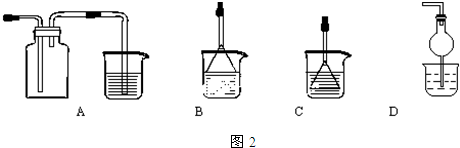
(4)制备CaCO3时,先通入 (填NH3或CO2),若实验过程中有氨气逸出,可选用图2装置中的 (填代号)装置吸收氨气.(烧杯中的液体都为水)

试回答下列问题:
(1)B物质的化学式是
A.KMnO4溶液 B.Fe粉 C. Na2CO3溶液 D. KSCN溶液
(2)向溶液A加入H2O2的作用是
(3)由溶液C获得CuSO4?5H2O,需要经过
(4)制备CaCO3时,先通入

考点:制备实验方案的设计
专题:实验设计题
分析:由制备实验流程可知,Cu2(OH)2CO3、少量Fe的氧化物均与硫酸反应,只有SiO2不反应,则B为SiO2,溶液A中含Cu2+、Fe2+、Fe3+,加H2O2的溶液将亚铁离子氧化为铁离子,则溶液B中含Cu2+、Fe3+,加CuO促进铁离子水解转化为沉淀,所以溶液C中主要为硫酸铜,蒸发浓缩、冷却结晶得到CuSO4?5H2O;
制备CaCO3时,先通入氨气,增大二氧化碳的溶解,生成碳酸铵与氯化钙反应生成碳酸钙、氯化铵,则过滤可得到CaCO3,以此来解答.
制备CaCO3时,先通入氨气,增大二氧化碳的溶解,生成碳酸铵与氯化钙反应生成碳酸钙、氯化铵,则过滤可得到CaCO3,以此来解答.
解答:
解:(1)Cu2(OH)2CO3、少量Fe的氧化物均与硫酸反应,只有SiO2不反应,则B为SiO2,检验铁离子,利用加KSCN溶液变为血红色即可,而A、B、C中物质不能检验铁离子,故答案为:SiO2;D;
(2)向溶液A加入H2O2将亚铁离子氧化为铁离子,其作用是氧化剂,离子反应方程式为H2O2+2Fe2++2H+=2Fe3++2H2O,选用H2O2而不用Cl2的原因是不引入新杂质Cl-,
故答案为:氧化;H2O2+2Fe2++2H+=2Fe3++2H2O;不引入新杂质Cl-;
(3)由溶液C获得CuSO4?5H2O,需要经过蒸发浓缩、冷却结晶、过滤等操作.除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器是玻璃棒,起引流作用,
故答案为:蒸发浓缩、冷却结晶;玻璃棒;
(4)要使CaCl2溶液中生成CaCO3,须在溶液显碱性的条件下通CO2,为使溶液显碱性,可向溶液中先通NH3;NH3极易溶于水,吸收多余NH3时要防止倒吸,图中B的倒扣漏斗、D的球形结构均可防止倒吸,A中气体收集时导管应短进,C中漏斗在液面下不能防止倒吸,
故答案为:NH3;BD.
(2)向溶液A加入H2O2将亚铁离子氧化为铁离子,其作用是氧化剂,离子反应方程式为H2O2+2Fe2++2H+=2Fe3++2H2O,选用H2O2而不用Cl2的原因是不引入新杂质Cl-,
故答案为:氧化;H2O2+2Fe2++2H+=2Fe3++2H2O;不引入新杂质Cl-;
(3)由溶液C获得CuSO4?5H2O,需要经过蒸发浓缩、冷却结晶、过滤等操作.除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器是玻璃棒,起引流作用,
故答案为:蒸发浓缩、冷却结晶;玻璃棒;
(4)要使CaCl2溶液中生成CaCO3,须在溶液显碱性的条件下通CO2,为使溶液显碱性,可向溶液中先通NH3;NH3极易溶于水,吸收多余NH3时要防止倒吸,图中B的倒扣漏斗、D的球形结构均可防止倒吸,A中气体收集时导管应短进,C中漏斗在液面下不能防止倒吸,
故答案为:NH3;BD.
点评:本题考查物质制备实验方案的设计,为高频考点,把握制备实验流程中的反应及混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意除杂不能引入新杂质及防倒吸装置的选择,题目难度中等.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
下列变化属于物理变化的是( )
| A、电解质溶液的导电 |
| B、石油裂解 |
| C、煤的干馏 |
| D、四氯化碳萃取碘水中的I2 |
在溶液中0.2mol X2O72-恰好能使0.6mol SO32-被完全氧化,则X2O72-被还原后X元素的化合价为( )
| A、+1 | B、+2 | C、+3 | D、+4 |
下列电离方程式错误的是( )
| A、AlCl3═Al3++3Cl- |
| B、Na2CO3═Na++CO32- |
| C、Ba(OH)2═Ba2++2OH- |
| D、BaSO4═Ba2++SO42- |
 在2L的密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L的密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表: