题目内容
19.已知:KSP[Fe(OH)2]=8.0×10-16,KSP[Fe(OH)3]=4.0×10-38.常温下,向1L含1.0molFe2(SO4)3和1.0molFeSO4的酸性混合溶液中通入NH3,至该溶液的pH为3时,溶液体积变化忽略不计,所得溶液中c(Fe2+):c(Fe3+)的值为( )| A. | 2:1 | B. | 1:1 | C. | 2.5×104:2 | D. | 2.5×104:1 |
分析 pH为3时,c(OH-)=10-11mol/L,结合Ksp(Fe(OH)2)=c(Fe2+)×c2(OH-)=8.0×10-16,Ksp(Fe(OH)3)=c(Fe3+)×c3(OH-)=4.0×10-38)计算c(Fe2+):c(Fe3+).
解答 解:pH为3时,c(OH-)=10-11mol/L,则1.0mol FeSO4溶液中c(Fe2+)×c2(OH-)=10-22<8.0×10-16,没有沉淀生成,则c(Fe2+)=1.0mol/L,
由Ksp(Fe(OH)3)=4.0×10-38可知,c(Fe3+)=$\frac{4.0×10{\;}^{-38}}{(1{0}^{-11}){\;}^{3}}$mol/L=4×10-5mol/L,则c(Fe2+):c(Fe3+)=1:4×10-5=2.5×104:1,
故选D.
点评 本题考查难溶电解质的溶解平衡,侧重于学生的分析、计算能力的考查,答题时注意把握溶度积的理解和运用,结合溶度积计算该题,难度不大.

练习册系列答案
相关题目
11.如图为周期表中的一部分,若a原子最外层电子数比次外层电子数少3个,则下列说法不正确 的是( )

| A. | a、b、c最高价氧化物对应的水化物的酸性强弱关系是c>b>a | |
| B. | a、b、c的氢化物水溶液的酸性强弱关系是a<b<c | |
| C. | a和d的原子结合可以形成带3个单位负电荷的阴离子 | |
| D. | 原子半径由大到小的顺序是c>b>d>a |
8.在一可变的密闭容器中进行反应:C(固)+H2O(气)?CO(气)+H2(气),下列条件的改变对反应速率几乎无影响的是:①增加C(固)的用量 ②将容器的体积缩小一半 ③保持体积不变,冲入N2,使体系的压强增大 ④保持压强不变,冲入N2,使容器的体积变大( )
| A. | ①④ | B. | ③④ | C. | ①③ | D. | ①③④ |
4.生活中的一些小常识往往包含化学知识,以下叙述不正确的是( )
| A. | 用食醋清除暖水瓶中的水垢 | |
| B. | 纤维素在人体内可水解为葡萄糖,故可作为人类的营养物质 | |
| C. | 用热的纯碱水洗涤油垢 | |
| D. | 葡萄糖中花青素在碱性环境下显紫色,故可用苏打粉打粉检验假红酒 |
11.下列关于热化学反应的描述中正确的是( )
| A. | HCl 和NaOH 反应的中和热△H=-57.3 kJ•mol-1,则 H2SO4 和Ca(OH)2 反应的中和热△H=2×(-57.3)kJ•mol-1 | |
| B. | 2CO2(g)═2CO(g)+O2(g)△H=+2×283.0 kJ•mol-1则 CO(g)的燃烧热是-283.0 kJ•mol-1 | |
| C. | 500℃、30 MPa下,0.5 mol N2(g)和1.5 mol H2(g)生成NH3(g)放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| D. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ 热量,氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ•mol-1 |
8.在一定温度下,容积一定的密闭容器中发生反应A(s)+2B(g)?C(g)+D(g),当下列物理量不再发生变化时,表明反应已达平衡的是( )
①混合气体的密度
②混合气体的压强
③B的物质的量浓度
④混合气体的总物质的量.
①混合气体的密度
②混合气体的压强
③B的物质的量浓度
④混合气体的总物质的量.
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①④ |
8.下列各组离子能再同一溶液中大量共存,用盐酸酸化后,溶液仍然澄清透明且颜色有变化的是( )
| A. | Na+、K+、SO32-、SO42- | B. | Na+、Ca2+、Cl-、CO32- | ||
| C. | Na+、K+、OH-、Al3+ | D. | Mg2+、Fe2+、NO3-、SO42- |
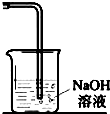 实验室常用以下方法制取氯气:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用.请你根据所学知识回答下列问题:
实验室常用以下方法制取氯气:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用.请你根据所学知识回答下列问题: