题目内容
将锌、铁、铜粉末按一定比例混合投入到一定量的硝酸中,微热,充分反应后过滤,弃去滤渣,滤液中 金属阳离子情况不可能是( )
A.只含 Cu2 +、Fe2+、Zn2+ B.只含 Zn2+
+、Fe2+、Zn2+ B.只含 Zn2+
C.只含 Fe2+、Zn2+ D.只含 Cu2+、Fe3+、Zn2+
练习册系列答案
相关题目
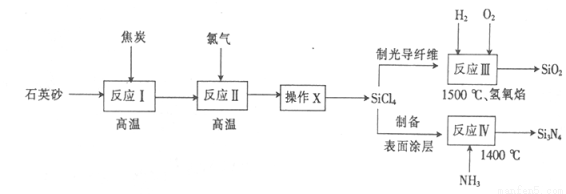
光纤通讯是光导纤维传送信号的一种通讯手段,合成光导纤维及氮化硅(一种无机涂层)的工艺流程如下:
回答下列问题:
(1)反应I的化学方程式为 ,氧化剂为 (填化学式)。
(2)经反应II所得的四氯化硅粗品中所含的物质如下:
组分名称 | SiCl4 | SiHCl3 | SiH2Cl2 | HCl | BCl3 | PCl3 |
质量分数 | 0.545 | 0.405 | 0.0462 | 0.0003 | 0.00193 | 0.00157 |
沸点/℃ | 57.6 | 31.8 | 8.2 | -85 | 12.5 | 75.5 |
图中“操作X”的名称为 ;PCl3的电子式为 。
(3)反应III和IV中尾气的用途为 ;反应IV的化学方程式为 。
1. 化学反应速率与化学平衡
化学反应速率与化学平衡
(一)恒温恒容下,将2molA气体和2molB气体通入体积为2L的密闭容器中发生如下反应:2A(g)+B(g)?x C(g)+2D(s),2min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mo1•L-1.
(1)从开始反应至达到平衡状态,A消耗的平均反应速率为0.4mol/(L•min).
(2)x=3.
(二)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应原理为:CO(g)+2H2(g)═CH3OH(g)△H,
下表所列数据是该反应在不同温度下的化学平衡常数(K).
①根据表中数据可判断△H<0 (填“>”、“=”或“<”),此反应较低(填“较高”或“较低”)温度下有利于该反应自发进行.
②在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将A.
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
③为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计的表中:
请在上表空格中填入剩余的实验条件数据.
(三)有平衡体系:CaCO3(s)?CaO(s)+CO2(g)中仅含有CaCO3、CaO及CO2.原压强为p,体积为V,在t0时间,将容器体积缩小为原来的一半并保持不变.若固体所占体积可忽略,且温度维持不变,在方框中画出t0时刻后体系中压强(p纵坐标)跟时间(t横坐标)的关系图.
 化学反应速率与化学平衡
化学反应速率与化学平衡(一)恒温恒容下,将2molA气体和2molB气体通入体积为2L的密闭容器中发生如下反应:2A(g)+B(g)?x C(g)+2D(s),2min时反应达到平衡状态,此时剩余1.2mol B,并测得C的浓度为1.2mo1•L-1.
(1)从开始反应至达到平衡状态,A消耗的平均反应速率为0.4mol/(L•min).
(2)x=3.
(二)能源短缺是人类社会面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.工业上合成甲醇的反应原理为:CO(g)+2H2(g)═CH3OH(g)△H,
下表所列数据是该反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
②在300℃时,将2mol CO、3mol H2和2mol CH3OH充入容积为1L的密闭容器中,此时反应将A.
A.向正方向移动 B.向逆方向移动 C.处于平衡状态 D.无法判断
③为了寻找合成甲醇的温度和压强的适宜条件,某同学设计了三组实验,部分实验条件已经填在下面实验设计的表中:
| 实验编号 | T(℃) | $\frac{n(CO)}{n({H}_{2})}$ | P(MPa) |
| i | 150 | $\frac{1}{3}$ | 0.1 |
| ii | 150 | $\frac{1}{3}$ | 5 |
| iii | 350 | $\frac{1}{3}$ | 5 |
(三)有平衡体系:CaCO3(s)?CaO(s)+CO2(g)中仅含有CaCO3、CaO及CO2.原压强为p,体积为V,在t0时间,将容器体积缩小为原来的一半并保持不变.若固体所占体积可忽略,且温度维持不变,在方框中画出t0时刻后体系中压强(p纵坐标)跟时间(t横坐标)的关系图.
5.下列关于金属腐蚀的说法正确的是( )
| A. | 金属在潮湿的空气中腐蚀的实质是:M+nH2O═M(OH)n+$\frac{n}{2}$H2↑ | |
| B. | 金属的化学腐蚀的实质是:M-ne-═Mn+,电子直接转移给还原剂 | |
| C. | 金属的化学腐蚀必须在酸性条件下进行 | |
| D. | 在潮湿的中性环境中金属的电化学腐蚀主要是吸氧腐蚀 |
6.将c mol•L-1的AlCl3溶液V1 mL加水稀释至V2 mL,稀释后溶液中Cl-物质的量浓度为( )
| A. | $\frac{{V}_{1}}{{V}_{2}}$c mol•L-1 | B. | $\frac{{V}_{1}}{{V}_{2}}$c mol•L-1 | ||
| C. | $\frac{{3V}_{2}}{{V}_{1}}$c mol•L-1 | D. | $\frac{3{V}_{1}}{{V}_{2}}$c mol•L-1 |


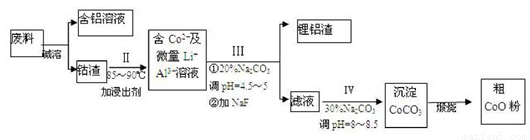
 钴以Co2O3 ·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。从废料中回收氧化钴(CoO)的工艺流程如下:
钴以Co2O3 ·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中。从废料中回收氧化钴(CoO)的工艺流程如下: