题目内容
1.海藻中含有丰富的碘元素(以I-形式存在).实验室中提取碘的流程如下: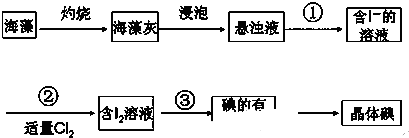
(1)实验操作③的名称是萃取分液,所用主要仪器名称为分液漏斗.
(2)提取碘的过程中,可供选择的有机试剂是BD(填序号).
A.酒精(沸点78℃) B.四氯化碳(沸点77℃)
C.甘油(沸点290℃) D.苯(沸点80℃)
(3)在操作②中,溶液中生成少量ICl,为消除此杂质,使碘全部游离出来,应加入适量(填序号)C溶液,反应的离子方程式ICl+I-=Cl-+I2.
A.KIO3 B.HClO C.KI D.Br2.
分析 (1)利用溶解性的差异来分析方法选择仪器;
(2)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多;
(3)操作②中生成碘,为除去ICl,应选择还原剂,生成碘且不引入新的杂质.
解答 解:(1)将碘水中的碘单质萃取出来,选择合适的萃取剂,采用萃取分液方法即可,选择分液漏斗分液,故答案为:萃取分液;分液漏斗;
(2)萃取的基本原则两种溶剂互不相溶,且溶质在一种溶剂中的溶解度比在另一种大的多,从题给信息可知,酒精、乙酸和水互溶,不能用作萃取剂,四氯化碳和苯与水互不相容,故可用四氯化碳或苯,故答案为:BD;
(3)操作②中生成碘,为除去ICl,ICl中I为+1价,应选择还原剂,生成碘且不引入新的杂质,最后选择KI,发生ICl+KI=KCl+I2,离子反应为ICl+I-=Cl-+I2,
故答案为:C;ICl+I-=Cl-+I2.
点评 本题主要考查海洋中的有用成分的提取方法及实验操作,明确发生的氧化还原反应及萃取分液操作是解答本题的关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.下列性质中不属于烷烃具有性质的是( )
| A. | 燃烧产物只有CO2和H2O | B. | 与溴水发生取代反应 | ||
| C. | 都难溶于水 | D. | 通常不与强酸、强碱、强氧化剂反应 |
2.mg甲烷燃烧后得到CO、CO2和H2O(g)组成的混合气体,其质量为14.4克.将其通过足量碱石灰后,气体质量变为2.8克.则混合气体中H2O的质量是多少( )
| A. | 3.6g | B. | 1.8g | C. | 7.2g | D. | 4.8g |
6.实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是( )
| A. | 锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度 | |
| B. | 滴定结束后,滴定管尖嘴处有一悬挂液滴 | |
| C. | 取NaOH溶液时先平视读数,后仰视读数 | |
| D. | 盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2次~3次 |
10.下列四个反应中,与其它三个反应类型不同的是( )
| A. | CH3CHO+H2$\stackrel{Ni}{→}$CH3CH2OH | |
| B. | CH3CHO+2Ag(NH3)2OH$\stackrel{△}{→}$CH3COONH4+2Ag↓+3NH3+H2O | |
| C. | CH3CHO+2Cu(OH)2+NaOH$\stackrel{△}{→}$CH3COONa+Cu2O↓+3H2O | |
| D. | 2CH3CHO+O2$\stackrel{△}{→}$2CH3COOH |
11.下列有关化学反应表达正确的是( )
| A. | 服用阿司匹林过量出现水杨酸(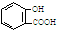 )中毒反应,可静脉注射NaHCO3溶液: )中毒反应,可静脉注射NaHCO3溶液: | |
| B. | 甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-$\stackrel{△}{→}$CO32-+2NH4++4Ag↓+6NH3+2H2O | |
| C. | 向CH2BrCOOH中加入足量的氢氧化钠溶液并加热:CH2BrCOOH+OH-$\stackrel{△}{→}$CH2BrCOO-+H2O | |
| D. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+2CO32- |
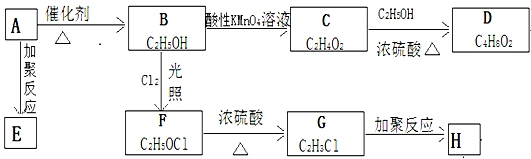
 ;
;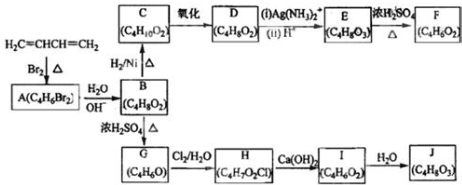
 ;
; +H2O,E中的官能团有羟基、羧基(填名称),与E具有相同官能团的E的同分异构体还有
+H2O,E中的官能团有羟基、羧基(填名称),与E具有相同官能团的E的同分异构体还有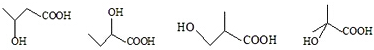 (写出结构简式,不考虑立体结构);
(写出结构简式,不考虑立体结构);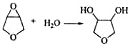 .
.