题目内容
下列有关化学用语表示正确的是( )
A、核内有8个中子的碳原子:
| ||
B、甲烷分子的比例模型: | ||
C、羟基的电子式: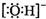 | ||
D、氯离子的结构示意图: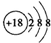 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.质量数=质子数+中子数,该碳原子的质量数为14,元素符号的左上角表示质量数、左下角表示质子数;
B.比例模型能够体现出分子的空间结构及各原子相对体积大小,据此判断甲烷的比例模型;
C.羟基为中性原子团,氧原子最外层为7个电子;
D.氯原子与氯离子的核电荷数相等,所以氯离子的核电荷数为17.
B.比例模型能够体现出分子的空间结构及各原子相对体积大小,据此判断甲烷的比例模型;
C.羟基为中性原子团,氧原子最外层为7个电子;
D.氯原子与氯离子的核电荷数相等,所以氯离子的核电荷数为17.
解答:
解:A.碳原子的核电荷数为6,核内有8个中子的碳原子的质量数为14,该原子正确的表示方法为:614C,故A错误;
B.甲烷为正四面体结构,碳原子半径大于氢原子,则甲烷的比例模型为: ,故B正确;
,故B正确;
C.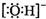 为氢氧根离子的电子式,羟基为中性原子团,氧原子最外层为7个电子,羟基正确的电子式为:
为氢氧根离子的电子式,羟基为中性原子团,氧原子最外层为7个电子,羟基正确的电子式为: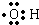 ,故C错误;
,故C错误;
D.氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构,氯离子正确的结构示意图为: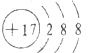 ,故D错误;
,故D错误;
故选B.
B.甲烷为正四面体结构,碳原子半径大于氢原子,则甲烷的比例模型为:
 ,故B正确;
,故B正确;C.
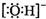 为氢氧根离子的电子式,羟基为中性原子团,氧原子最外层为7个电子,羟基正确的电子式为:
为氢氧根离子的电子式,羟基为中性原子团,氧原子最外层为7个电子,羟基正确的电子式为: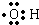 ,故C错误;
,故C错误;D.氯离子的核电荷数为17,核外电子总数为18,最外层达到8电子稳定结构,氯离子正确的结构示意图为:
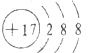 ,故D错误;
,故D错误;故选B.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握电子式、比例模型、离子结构示意图、元素符号等化学用语的概念及正确的表示方法,明确原子结构示意图与离子结构示意图的区别,试题培养了学生规范答题的能力.

练习册系列答案
相关题目
25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A、0.1mol?L-1 AlC13溶液中:H+、Na+、Cl-、SO42- |
| B、含有0.1mol?L-1 Fe3+的溶液中:Na+、K+、SCN-、NO3- |
| C、使甲基橙变红色的溶液中:Fe2+、K+、NO3-、SO42- |
| D、由水电离产生的c(H+)=10-12 mol?L-1的溶液中:NH4+、SO42-、HCO3-、Cl- |
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、1mol CH3+所含电子数目为6NA |
| B、7.8 g Na2O2含有阴离子数目为0.2NA |
| C、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移电子数为NA |
| D、1mol NaHSO4晶体含阳离子数为2NA |
当光束通过下列分散系是,能观察到丁达尔效应的是( )
| A、硫酸 |
| B、澄清石灰水 |
| C、Fe(OH)3胶体 |
| D、石灰乳 |
如图是CH4、CCl4、CH3Cl的分子球棍模型图.下列说法正确的是( )
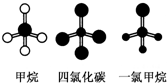

| A、CH4、CCl4和CH3Cl都是正四面体结构 |
| B、CH4、CCl4都是正四面体结构 |
| C、CH4和CCl4中的化学键完全相同 |
| D、CH4、CCl4的结构相同,性质也相同 |
下列指定反应的离子方程式正确的是( )
| A、向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O→C6H5OH+HCO3- | ||||
| B、AlCl3溶液中加入少量氨水:Al3++3OH-=Al(OH)3↓ | ||||
| C、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-=Fe(OH)2↓ | ||||
D、用惰性电极电解氯化钠溶液:2Cl-+2H+
|
下列化学式代表的物质一定有固定沸点的是( )
| A、C3H6 |
| B、C2H4O2 |
| C、CF2Cl2 |
| D、C3H7OH |
不能使橙黄色溴水变成无色溶液的是( )
| A、锌粉 |
| B、用四氯化碳多次萃取 |
| C、氢氧化钾溶液 |
| D、碘化钾溶液 |
对比饱和链烃、不饱和链烃的结构和性质,苯的独特性质具体来说是( )
| A、难氧化,易加成,难取代 |
| B、易取代,能加成,难氧化 |
| C、易氧化,易加成,难取代 |
| D、因是单双键交替结构,故易加成为环己烷 |