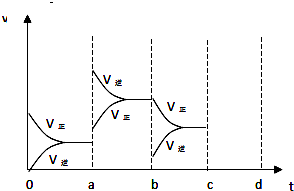题目内容
高温下,某反应达到平衡,平衡常数K=
.恒容时,温度升高,H2浓度减小.下列说法正确的是( )
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| A、该反应是焓变为正值 | |||
| B、增大压强,H2浓度一定减小 | |||
| C、升高温度,逆反应速率减小 | |||
D、该反应化学方程式为CO+H2O
|
考点:化学平衡的影响因素
专题:化学平衡专题
分析:化学平衡常数,是指在一定温度下,可逆反应达到平衡时,各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,某反应达到平衡,平衡常数K=
,可知该可逆反应为CO2(g)+H2(g)?CO(g)+H2O(g),恒容时,温度升高,H2的浓度减小,说明平衡向正反应移动,该反应正反应为吸热反应.
A、恒容时,温度升高,H2的浓度减小,说明平衡向正反应移动,升高温度平衡向吸热反应移动;
B、该反应前后气体的体积不发生变化,恒温恒容时,加入不反应的气体,增大压强,平衡不移动,H2的浓度不变;增大氢气的浓度,增大压强,平衡向正反应移动,平衡是氢气的浓度增大,与增大压强的方法有关;
C、升高温度,反应物、生成物的活化分子增多,正、逆反应速率都增大;
D、反应达到平衡,平衡常数K=
,可知该可逆反应为CO2(g)+H2(g)?CO(g)+H2O(g).
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
A、恒容时,温度升高,H2的浓度减小,说明平衡向正反应移动,升高温度平衡向吸热反应移动;
B、该反应前后气体的体积不发生变化,恒温恒容时,加入不反应的气体,增大压强,平衡不移动,H2的浓度不变;增大氢气的浓度,增大压强,平衡向正反应移动,平衡是氢气的浓度增大,与增大压强的方法有关;
C、升高温度,反应物、生成物的活化分子增多,正、逆反应速率都增大;
D、反应达到平衡,平衡常数K=
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
解答:
解:A、恒容时,温度升高,H2的浓度减小,说明平衡向正反应移动,该反应正反应为吸热反应,即反应的焓变为正值,故A正确;
B、恒温恒容时,增大氢气的浓度,增大压强,平衡向正反应移动,平衡时氢气的浓度增大,故B错误;
C、升高温度,反应物、生成物的活化分子增多,正、逆反应速率都增大,故C错误;
D、平衡常数K=
,可知该可逆反应为CO2(g)+H2(g)?CO(g)+H2O(g),故D错误.
故选A.
B、恒温恒容时,增大氢气的浓度,增大压强,平衡向正反应移动,平衡时氢气的浓度增大,故B错误;
C、升高温度,反应物、生成物的活化分子增多,正、逆反应速率都增大,故C错误;
D、平衡常数K=
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
故选A.
点评:本题考查外界条件对化学平衡的影响、化学平衡常数等,难度中等,注意对化学平衡常数的理解,同一反应,化学计量数不同,平衡常数不同.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
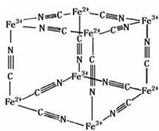 普鲁士蓝晶体结构如下图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )
普鲁士蓝晶体结构如下图所示(每两个立方体中,一个K+在其中一个立方体中心,另一个则无K+),下列说法正确的是( )| A、化学式可以表示为KFe2(CN)6 |
| B、一个立方体中含有12个π键 |
| C、普鲁士蓝中含有配位键 |
| D、Fe3+周围有12个Fe2+离子 |
在一定温度下的刚性密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:A(s)+2B(g)?C(g)+D(g)已达到平衡状态( )
| A、混合气体的压强 |
| B、混合气体的体积 |
| C、各气体物质的物质的量浓度 |
| D、气体的总物质的量 |
下列现象不能用“相似相溶规则”原理解释的是( )
| A、氯化氢易溶于水 |
| B、氯气易溶于氢氧化钠溶液 |
| C、碘易溶于四氯化碳 |
| D、碘难溶于水 |
某同学通过系统实验探究铝及其化合物的性质,操作正确且能达到目的是( )
| A、用互相滴加的方法可鉴别氯化铝溶液、氢氧化钠溶液 |
| B、向氯化铝溶液中滴加过量氨水,最终得到澄清溶液 |
| C、常温下铝与浓硝酸反应制得大量的NO2 |
| D、AlCl3溶液加热蒸干得到无水氯化铝晶体 |
 某学生用0.10mol/L标准NaOH溶液滴定某浓度的盐酸.记录数据如下:
某学生用0.10mol/L标准NaOH溶液滴定某浓度的盐酸.记录数据如下: