题目内容
决定化学反应速率的主要因素是( )
| A、反应物的浓度 |
| B、反应体系内的压强 |
| C、反应物的性质 |
| D、反应物的状态 |
考点:化学反应速率的影响因素
专题:化学反应速率专题
分析:决定化学反应速率的主要因素是反应物的内因,即物质的性质,而温度、浓度、压强以及催化剂为外界因素.
解答:
解:影响化学反应速率的因素有内因和外因,内因为反应物的性质,是决定化学反应速率的主要因素,外因有温度、浓度、压强以及催化剂等,为次要因素.
故选C.
故选C.
点评:本题考查影响化学反应速率的因素,为高频考点,侧重于基础知识的综合理解和运用的考查,题目难度不大,注意影响化学反应速率的主要原因是物质的性质.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在水溶液中,重铬酸钾K2Cr2O7存在以下平衡:Cr2
+H2O?2Cr
+2H+,下列说法正确的是( )
| O | 2- 7 |
| O | 2- 4 |
| A、向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色 | ||||||
| B、该反应不是氧化还原反应 | ||||||
| C、向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大 | ||||||
D、该反应的平衡常数表达式是K=
|
下列反应中,属于放热反应的是( )
①NaOH溶液中加入盐酸 ②C与CO2反应生成CO ③铝热反应 ④由氯酸钾制O2.
①NaOH溶液中加入盐酸 ②C与CO2反应生成CO ③铝热反应 ④由氯酸钾制O2.
| A、①② | B、②③ | C、①③ | D、①④ |
能正确表示下列反应的离子方程式的是( )
| A、将Cl2通入氯化亚铁溶液:Fe2++Cl2=Fe3++2Cl- |
| B、铜与浓硝酸的反应:Cu+4HNO3(浓)=Cu2++2NO3-+2NO2↑+2H2O |
| C、Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| D、向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2Fe3++2 Br2+6Cl- |
下列各项中,与主族元素在元素周期表中所处位置有关的是( )
| A、相对原子质量 |
| B、电子层数和最外层电子数 |
| C、次外层电子数 |
| D、核内中子数 |
下列离子方程式不正确的是( )
| A、用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32- |
| B、向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液使SO42-沉淀完全:2Ba2++NH4++Al3++2SO42-+4OH-=Al(OH)3↓+2BaSO4↓+NH3?H2O |
| C、Cl2与FeI2溶液反应,当n(Cl2):n(FeI2)=1:1时,2Fe2++2I-+2Cl2=2Fe3++2I2+4Cl- |
| D、将1mol/L NaAlO2溶液和1.5mol/L HCl溶液等体积互相均匀混合:6AlO2-+9H++3H2O=5Al(OH)3↓+Al3+ |
下列实验可行的是( )
| A、用澄清石灰水检验CO中含有的CO2 |
| B、用BaCl2除去NaOH溶液中混有的少量Na2SO4 |
| C、用乙醇从碘水中萃取碘 |
| D、用溶解、过滤的方法分离CaCl2和NaCl固体混合物 |
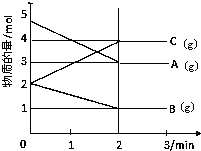 某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.
某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示. 按如图所示操作,充分反应后:
按如图所示操作,充分反应后: