题目内容
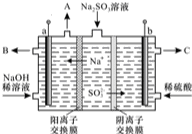
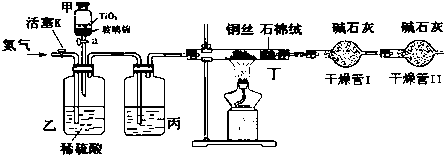
18.亚硝酸钠被称为工业盐,在漂白、电镀等方面应用广泛.以木炭,浓硝酸、水和铜为原料生成的一氧化氮与过氧化钠反应制备亚硝酸钠的装置如图所示.已知:室温下,①2NO+Na2O=2NaNO2
②酸性条件下,NO或NO2-都能与MnO4-反应生成NO3-和Mn2+,
5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O
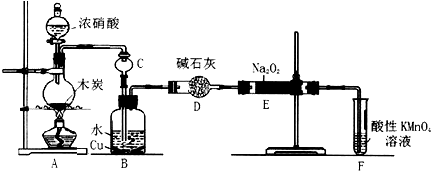
(1)A中观察到的现象是有红棕色气体生成 或 有(深)红色气体生成
(2)装置B中反应的离子方程式有3NO2+H2O=2H++2NO3-+NO、3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O.
(3)装置C的作用是防止倒吸,装置F的作用是吸收未反应的NO
(4)若无装置D,则E中产物除亚硝酸钠外还含有副产物Na2CO3NaOH.(填化学式)
(5)NaNO2像食盐一样的咸味,但能引起中毒.已知亚硝酸钠能发生如下反应:
2NaNO2+4HI=2NO+I2+2NaI+2H2O,根据上述反应,可以用试剂和生活中常见的物质进行实验,以鉴别亚硝酸钠和食盐.进行实验时,必须选用的物质有BE.
A、自来水 B、碘化钾淀粉试液 C、淀粉 D、白糖 E、食醋 F、白酒
(6)充分反应后,某同学设计实验对E中NaNO2的含量进行检测.称取E中固体2g,完全溶解配制成溶液100mL,取出25mL溶液用0.100mol/L酸性KMnO4溶液进行滴定(杂质不与KMnO4反应),消耗KMnO4溶液20mL,求样品中亚硝酸钠的质量分数69.0%(保留小数点后1位)(已知:NaNO2摩尔质量为69g/mol)
分析 装置A中是浓硝酸和碳加热发生的反应,反应生成二氧化氮和二氧化碳和水,装置B中是A装置生成的二氧化氮和水反应生成硝酸和一氧化氮,硝酸和铜反应生成硝酸铜,一氧化氮和水;通过装置E中的过氧化钠吸收一氧化氮、二氧化碳,最后通过酸性高锰酸钾溶液除去剩余一氧化氮防止污染空气.
(1)A中生成二氧化氮;
(2)二氧化氮与水反应生成硝酸,铜能与稀硝酸反应;
(3)大肚瓶可防止倒吸,酸性高锰酸钾溶液可吸收未反应的NO;
(4)二氧化碳和过氧化钠发生的反应生成碳酸钠和氧气,水与过氧化钠反应生成氢氧化钠;
(5)鉴别NaNO2和NaCl,利用2NaNO2+4HI═2NO+I2+2NaI+2H2O及碘遇淀粉变蓝分析;
(6)根据方程式5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O可求出亚硝酸钠的物质的量,然后求样品中亚硝酸钠的质量分数.
解答 解:装置A中是浓硝酸和碳加热发生的反应,反应生成二氧化氮和二氧化碳和水,装置B中是A装置生成的二氧化氮和水反应生成硝酸和一氧化氮,硝酸和铜反应生成硝酸铜,一氧化氮和水;通过装置E中的过氧化钠吸收一氧化氮、二氧化碳,最后通过酸性高锰酸钾溶液除去剩余一氧化氮防止污染空气.
(1)根据装置图可知,A中浓硝酸与木炭发生氧化还原反应生成CO2和NO2以及水,因此A中观察到的现象有红棕色气体生成,
故答案为:有红棕色气体生成 或 有(深)红色气体生成;
(2)NO2溶于水生成NO和硝酸,硝酸具有氧化性能把金属铜氧化,则装置B中反应的离子方程式有3NO2+H2O=2H++2NO3-+NO、3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O,
故答案为:3NO2+H2O=2H++2NO3-+NO、3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O;
(3)NO2极易溶于水与水反应,所以装置C的作用是防止倒吸;NO与过氧化钠反应后有剩余,随意排放容易引起大气污染,而NO能被酸性高锰酸钾溶液氧化,则装置F的作用吸收未反应的NO,故答案为:防止倒吸;吸收未反应的NO;
(4)生成的NO中含有CO2和水蒸气,二者均能与过氧化钠反应,而碱石灰可以吸收CO2和水蒸气,所以如果没有D装置,则E中产物除亚硝酸钠外还含有副产物Na2CO3、NaOH,故答案为:Na2CO3、NaOH;
(5)鉴别NaNO2和NaCl,由2NaNO2+4HI═2NO+I2+2NaI+2H2O及碘遇淀粉变蓝可知,则选择试剂为BE,
故答案为:BE;
(6)消耗高锰酸钾的物质的量是0.1mol/L×0.02L=0.002mol,则根据方程式5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O可知,亚硝酸钠的物质的量是0.002mol×$\frac{5}{2}$=0.005mol,则原样品中亚硝酸钠的物质的量是0.005mol×$\frac{100mL}{25mL}$=0.02mol,其质量为0.02mol×69g/mol=1.38g,所以样品中亚硝酸钠的质量分数$\frac{1.38g}{2g}$×100%=69.0%,
故答案为:69.0%.
点评 本题考查硝酸的性质、尾气处理、实验条件控制、实验方案设计与评价以及物质含量测定,注意实验过程中的反应现象分析,掌握基础是关键,题目难度中等.

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案(1)实验室利用反应TiO2(s)+CCl4(g)$\frac{\underline{\;△\;}}{\;}$TiCl4(g)+CO2(g),在无水无氧条件下,制取TiCl4实验装置示意图如图:
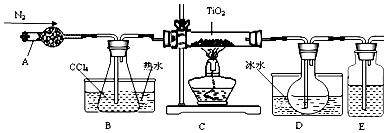
有关物质性质如表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾 |
②欲分离D中的液态混合物,所采用操作的名称是蒸馏.
(2)工业上可以由钛铁矿(FeTiO3)(含Fe2O3等杂质)制备金属Ti.
工业制备过程由钛铁矿经过酸溶解、过滤以及后续一系列化学变化和物理变化,可以将不溶于水的H2TiO3从溶液中过滤出来,再对H2TiO3进行洗涤,最后对H2TiO3进行煅烧得到TiO2,最终获得金属Ti.过程简化如下:
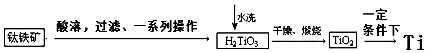
①水洗H2TiO3后,向洗涤液中加滴加KSCN溶液后无明显现象,再加H2O2后出现微红色,说明H2TiO3中存在的杂质离子是Fe2+.
用离子方程式解释“出现微红色”的原因2Fe2++H2O2+2H+=2Fe3++2H2O,Fe3++3SCN-=Fe(SCN)3
②以TiO2为原料制取金属钛的其中一步反应为TiO2、氯气和焦炭反应生成TiCl4,己知该反应中氧化剂与还原剂的物质的量之比为1:1,则另一生成物为CO.
③用Mg还原TiCl4制金属钛取过程中必须在1070K的温度下进行,你认为还应该控制的反应条件是隔绝空气(或惰性气氛中);
所得到的金属钛中混有少量杂质,可加入稀盐酸或稀硫酸溶解后除去.
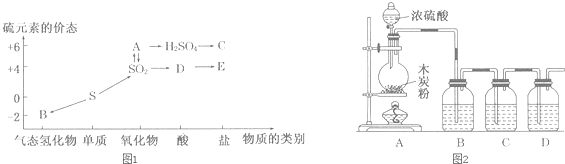
 硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾.
硫酸厂用煅烧黄铁矿(FeS2)来制取硫酸,实验室利用硫酸厂烧渣(主要成分是Fe2O3及少量FeS、SiO2)制备绿矾.
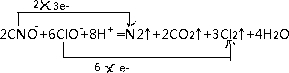 .
.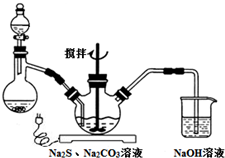 NaCN为剧毒无机物.某兴趣小组查资料得知,实验室里的NaCN溶液可用Na2S2O3溶液进行解毒销毁,他们开展了以下三个实验,请根据要求回答问题:
NaCN为剧毒无机物.某兴趣小组查资料得知,实验室里的NaCN溶液可用Na2S2O3溶液进行解毒销毁,他们开展了以下三个实验,请根据要求回答问题: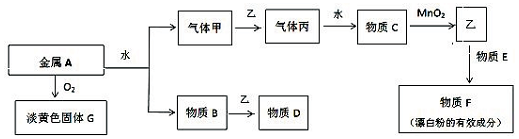
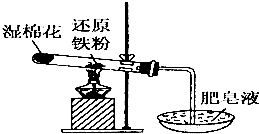 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应.小明设计如下实验探究铁粉与水蒸气反应后的气体产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应.小明设计如下实验探究铁粉与水蒸气反应后的气体产物.