题目内容
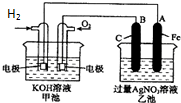 如图是一个化学过程的示意图.已知甲池的总反应式为:2H2+O2═2H2O
如图是一个化学过程的示意图.已知甲池的总反应式为:2H2+O2═2H2O(1)请回答:
甲电池是
(2)写出下列电极反应式:
通入H2的电极的电极反应式是
A(Fe)电极的电极反应式为
(3)乙池中反应的化学方程式为
(4)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上转移电子
考点:原电池和电解池的工作原理
专题:
分析:甲池为原电池,通入氢气的一极为原电池的负极,通入氧气的一极为原电池的正极,乙池为电解池,石墨为阳极,发生氧化反应,Fe极为电解池的阴极,发生还原反应,以此解答该题.
解答:
解:(1)根据反应方程式知,甲装置是一个燃料电池,所以甲是把化学能转变为电能的装置,是原电池;乙有外加电源,所以是电解池.氢气发生氧化反应,所以该电极是负极,O2 发生还原反应,所以该电极是正极;石墨与原电池的正极相连,所以石墨电极B是阳极;
故答案为:原电池;阳极;
(2)通入H2的电极为负极,发生氧化反应,电极方程式为2H2-4e-+4OH-═4H2O,Fe为电解池的阴极,银离子得电子被还原,电极方程式为4Ag++4e-═4Ag(或Ag++e-═Ag),
故答案为:2H2-4e-+4OH-═4H2O;4Ag++4e-═4Ag(或Ag++e-═Ag);
(3)乙池中离子放电顺序为:阳离子 Ag+>H+,阴离子OH->NO3 -,阴极电极反应为:O2+2H2O+4e-=4OH-;阳极电极反应为:4Ag++4e-=4Ag;依据电子守恒和电解的实质写出化学方程式:4AgNO3+2H2O
4Ag+O2↑+4HNO3,
故答案为:4AgNO3+2H2O
4Ag+O2↑+4HNO3;
(4)乙池中A(Fe)极发生Ag++e-═Ag,质量增加5.40g时,n(Ag)=
=0.05mol,转移0.05mol电子,
故答案为:0.05.
故答案为:原电池;阳极;
(2)通入H2的电极为负极,发生氧化反应,电极方程式为2H2-4e-+4OH-═4H2O,Fe为电解池的阴极,银离子得电子被还原,电极方程式为4Ag++4e-═4Ag(或Ag++e-═Ag),
故答案为:2H2-4e-+4OH-═4H2O;4Ag++4e-═4Ag(或Ag++e-═Ag);
(3)乙池中离子放电顺序为:阳离子 Ag+>H+,阴离子OH->NO3 -,阴极电极反应为:O2+2H2O+4e-=4OH-;阳极电极反应为:4Ag++4e-=4Ag;依据电子守恒和电解的实质写出化学方程式:4AgNO3+2H2O
| ||
故答案为:4AgNO3+2H2O
| ||
(4)乙池中A(Fe)极发生Ag++e-═Ag,质量增加5.40g时,n(Ag)=
| 5.4g |
| 108g/mol |
故答案为:0.05.
点评:本题考查了原电池和电解池原理,为高频考点,侧重于学生的分析能力和计算能力的考查,明确离子放电顺序是解本题关键,难点是电极反应式的书写,题目难度中等.

练习册系列答案
相关题目
下列试剂中,可将乙醇、淀粉溶液和苯三种无色液体鉴别开的是( )
| A、氢氧化钠 |
| B、新制Cu(OH)2浊液 |
| C、溴水 |
| D、碘水 |
在一定温度下,氯化银在水中存在如下沉淀溶解平衡:AgCl(s)?Ag+(aq)+Cl-(aq),若把AgCl分别放入①100mL0.1mol/LNa2SO4溶液中;②100mL0.1mol/L NaCl溶液中;③100mL0.1mol/L AlCl3溶液中;④100mL0.1mol/L MgCl2溶液中.搅拌后在相同的温度下Ag+浓度由大到小的顺序是( )
| A、①>②>④>③ |
| B、②>①>④>③ |
| C、④>③>②>① |
| D、①>④>③>② |
下列实验操作错误的是( )
A、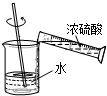 稀释浓硫酸 |
B、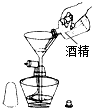 添加酒精 |
C、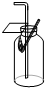 氧气验满 |
D、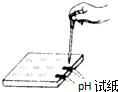 测溶液pH |
对于淀粉和纤维素两种物质,下列说法正确的是( )
| A、二者都能水解,水解的最终产物不同 |
| B、二者C、H、O三种元素的质量分数相同,且互为同分异构体 |
| C、它们都是糖类,且都是高分子化合物 |
| D、都可用(C6H10O5)n表示,但淀粉能发生银镜反应,而纤维素不能 |