题目内容
 如图是实验室利用无水乙醇、冰醋酸和浓硫酸制备乙酸乙酯的实验装置.试回答:
如图是实验室利用无水乙醇、冰醋酸和浓硫酸制备乙酸乙酯的实验装置.试回答:(1)乙酸分子中官能团的名称是
(2)写出甲中反应的化学方程式
(3)小试管乙中饱和Na2CO3溶液的主要作用是
(4)可用
考点:乙酸乙酯的制取
专题:实验设计题
分析:(1)乙酸的官能团是羧基;
(2)甲中发生酯化反应,羧酸脱去的是羟基,反应方程式为C2H5OH+CH3COOH
CH3COOC2H5+H2O;
(3)在饱和碳酸钠溶液中,乙酸乙酯的溶解度较低,且能够溶解乙醇,反应掉乙酸;
(4)由于乙酸乙酯的沸点低,可用蒸馏的方法蒸出乙酸乙酯;
(2)甲中发生酯化反应,羧酸脱去的是羟基,反应方程式为C2H5OH+CH3COOH
| 浓硫酸 |
| △ |
(3)在饱和碳酸钠溶液中,乙酸乙酯的溶解度较低,且能够溶解乙醇,反应掉乙酸;
(4)由于乙酸乙酯的沸点低,可用蒸馏的方法蒸出乙酸乙酯;
解答:
解:(1)乙酸的官能团是羧基,故答案为:羧基;
(2)甲中发生酯化反应,羧酸脱去的是羟基,反应方程式为C2H5OH+CH3COOH
CH3COOC2H5+H2O;
故答案为:C2H5OH+CH3COOH
CH3COOC2H5+H2O;
(3)在饱和碳酸钠溶液中,乙酸乙酯的溶解度较低,且能够溶解乙醇,反应掉乙酸,
故答案为:降低乙酸乙酯的溶解度;吸收乙醇;除去乙酸;
(4)由于乙酸乙酯的沸点低,可用蒸馏的方法蒸出乙酸乙酯;故答案为:蒸馏.
(2)甲中发生酯化反应,羧酸脱去的是羟基,反应方程式为C2H5OH+CH3COOH
| 浓硫酸 |
| △ |
故答案为:C2H5OH+CH3COOH
| 浓硫酸 |
| △ |
(3)在饱和碳酸钠溶液中,乙酸乙酯的溶解度较低,且能够溶解乙醇,反应掉乙酸,
故答案为:降低乙酸乙酯的溶解度;吸收乙醇;除去乙酸;
(4)由于乙酸乙酯的沸点低,可用蒸馏的方法蒸出乙酸乙酯;故答案为:蒸馏.
点评:本题考查了乙酸乙酯的制取,注意浓硫酸和饱和碳酸钠溶液的作用,本题注重了教材基础知识,难度不高.

练习册系列答案
相关题目
已知短周期元素X、Y、Z在元素周期表中的位置如图,下列说法正确的是( )


| A、原子半径Z>Y>X |
| B、X元素属于第2周期 |
| C、气态氢化物的稳定性:X>Y>Z |
| D、最高价氧化物水化物的酸性:Y>Z>X |
下列有关实验现象或操作预测的叙述正确的是( )
A、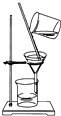 可用于分离乙醇和水 |
B、 说明该装置气密性良好 |
C、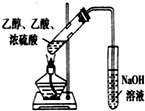 该装置可用于制取并收集乙酸乙酯 |
D、 由a进气可用于收集NH3 |
下列操作不能达到目的是( )
A、 制取CO2 |
B、 收集氯气 |
C、 检查气密性 |
D、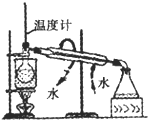 I2的乙醚溶液中分离I2 |
下列有关物质性质或应用的说法正确的是( )
| A、蛋白质水解生成葡萄糖放出热量,提供生命活动的能量 |
| B、次氯酸钠具有强还原性,可用于配制消毒液 |
| C、氯气和二氧化硫都具有漂白性,两者混合使用能提高漂白的效率 |
| D、碳酸钠溶液显碱性,用热的饱和碳酸钠溶液可除去金属表面的油污 |
下列各组离子中,能在溶液中大量共存的是( )
| A、H+、Ca2+、Cl-、CO32- |
| B、I-、ClO-、K+、H+ |
| C、Na+、Fe3+、SO42-、OH- |
| D、Na+、Cu2+、Cl-、SO42- |
 ,链烃A能发生如图所示的一系列变化:
,链烃A能发生如图所示的一系列变化:
