题目内容
白磷(P4)分子是正四面体形,4个P原子位于正四面体的四个顶点,如下图所示。
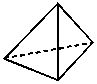
(1)分子中P―P键之间的夹角是_________。
(2)1molP4分子中含有__________molP―P键。
(3)P―P键是__________键(填“非极性”或“极性”)。
见解析
【试题分析】
(1)根据题目给出的信息可知,白磷是正四面体形分子,则四个面均为由三个磷原子构成的正三角形,内角均是60°,即P―P键之间的夹角为60°。
(2)P4分子为正四面体形,观察其结构知,一个P4分子有6条棱,即6个化学键(P―P),则1molP4分子中含有6molP―P键。
(3)P―P键由同种元素的原子组成,两元素的电负性相同,两个P原子吸引电子的能力相同,共用电子对不偏向其中任何一个原子,则P―P键是非极性键。

练习册系列答案
相关题目
下列说法正确的是:

A.电子从3S能级跃迁到3P能级形成的光谱是发射光谱 | B.白磷(P4)分子是正四面体结构,故分子中的键角为1090281 | C.NO2-中心原子采取sp2杂化,分子空间构型为“V”形 | D.原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低 |
 A.电子从3S能级跃迁到3P能级形成的光谱是发射光谱
A.电子从3S能级跃迁到3P能级形成的光谱是发射光谱