题目内容
下列说法正确的是( )
| A、含有离子键的化合物一定是离子化合物 |
| B、含有共价键的化合物一定是共价化合物 |
| C、全部由非金属元素组成的化合物一定是共价化合物 |
| D、H2SO4溶于水能电离出H+和SO42-,所以H2SO4是离子化合物 |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:A.离子化合物中一定含有离子键,可能含有共价键;
B.含有共价键的化合物可能是离子化合物;
C.全部由非金属元素组成的化合物可能是离子化合物;
D.硫酸是共价化合物.
B.含有共价键的化合物可能是离子化合物;
C.全部由非金属元素组成的化合物可能是离子化合物;
D.硫酸是共价化合物.
解答:
解:A.含有离子键的化合物是离子化合物,离子化合物中一定含有离子键,可能含有共价键,故A正确;
B.含有共价键的化合物可能是离子化合物,如KOH,故B错误;
C.全部由非金属元素组成的化合物可能是离子化合物,如铵盐,故C错误;
D.硫酸分子中O原子和H原子、S原子和O原子之间只存在共价键,所以硫酸中只含共价键,是共价化合物,故D错误;
故选A.
B.含有共价键的化合物可能是离子化合物,如KOH,故B错误;
C.全部由非金属元素组成的化合物可能是离子化合物,如铵盐,故C错误;
D.硫酸分子中O原子和H原子、S原子和O原子之间只存在共价键,所以硫酸中只含共价键,是共价化合物,故D错误;
故选A.
点评:本题考查了化合物类型的判断,根据物质的构成微粒确定化合物类型,易错选项是C,不能根据是否含有金属元素判断化合物类型,为易错点.

练习册系列答案
相关题目
柠檬烯是一种食用香料,其结构简式如图,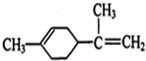 有关柠檬烯的分析不正确的是( )
有关柠檬烯的分析不正确的是( )
 有关柠檬烯的分析不正确的是( )
有关柠檬烯的分析不正确的是( )| A、柠檬烯的核磁图谱中能出现8个峰 |
| B、柠檬烯的同分异构体中属于芳香族的有12种 |
| C、柠檬烯的分子中所有的碳原子不可能在同一个平面上 |
| D、在一定条件下,柠檬烯可以发生加成、氧化、加聚等反应 |
 石墨烯(graphene)是目前科技研究的热点,可看作将石墨的层状结构一层一层的剥开得到的单层碳原子.将氢气加入到石墨烯排列的六角晶格中可得最薄的导电材料石墨烷(graphane,如图),下列说法中正确的是(NA表示阿伏伽德罗常数)( )
石墨烯(graphene)是目前科技研究的热点,可看作将石墨的层状结构一层一层的剥开得到的单层碳原子.将氢气加入到石墨烯排列的六角晶格中可得最薄的导电材料石墨烷(graphane,如图),下列说法中正确的是(NA表示阿伏伽德罗常数)( )| A、石墨烯与石墨烷互为同素异形体 |
| B、石墨烯转变为石墨烷可看作取代反应 |
| C、12g石墨烯所含碳碳键数目为1.5NA |
| D、12g石墨烯完全转变为石墨烷需氢气11.2L |
下列表示物质结构的化学用语或模型图正确的是( )
| A、乙醇的分子式:CH3CH2OH | ||
B、二氧化碳的电子式: | ||
C、乙烷的球棍模型 | ||
D、中子数为20的氯原子:
|
下列物质中,不能由Fe跟非金属单质直接化合而成的是( )
| A、Fe3O4 |
| B、FeS |
| C、FeCl3 |
| D、FeCl2 |
下列说法一定正确的是( )
| A、周期表中同主族元素单质的熔点从上到下逐渐增高 |
| B、16g石墨与8g CH4所含共价键数目相等 |
| C、钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水 |
| D、若将AlCl3溶液、Na2SO3溶液蒸干并灼烧可分别得到AlCl3和Na2SO3 |
下列物质中既含有共价键又含离子键的化合物是( )
| A、MgCl2 |
| B、NaOH |
| C、K2O |
| D、C6H6 |
一种基于酸性燃料电池原理设计的酒精检测仪,电池反应的化学方程式为:CH3CH2OH+O2═CH3COOH+H2O.下列有关说法正确的是( )
| A、检测时,电解质溶液中的H+向负极移动 |
| B、若有0.4mol电子转移,则在标准状况下消耗4.48L氧气 |
| C、负极上的反应为:CH3CH2OH-4e-+H2O═CH3COOH+4H+ |
| D、正极上发生的反应为:O2+4e-+2H2O═4OH- |
某有机物的结构简式为: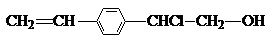
①可以燃烧②能使酸性高锰酸钾溶液褪色③能与NaOH溶液反应④能发生消去反应⑤能发生加聚反应( )
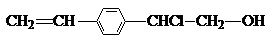
①可以燃烧②能使酸性高锰酸钾溶液褪色③能与NaOH溶液反应④能发生消去反应⑤能发生加聚反应( )
| A、只有①③ | B、只有②④⑤ |
| C、除③外 | D、全部 |