题目内容
12.卫生部公布了食盐碘含量的标准,规定每千克碘含量不超30毫克,2012年3月15日起实施.氯化钠既是一种重要的生活必需品,也是重要的化工原料.下列说法正确的是( )| A. | 食用加碘盐可预防碘缺乏症,加碘盐中加的含碘物质是碘单质 | |
| B. | 因为NaCl的水溶液能导电,所以NaCl溶液属于强电解质 | |
| C. | 电解熔融NaCl得到23.0g金属钠时能产生22.4 L氯气(标准状况下) | |
| D. | 37Cl 是氯元素的一种同位素,23Na37Cl中质子数和中子数之比是7:8 |
分析 A.食用加碘盐可预防碘缺乏症,加碘盐中加的含碘物质是碘酸钾;
B.电解质是化合物,NaCl溶液是混合物;
C.利用电解反应中氯化钠的物质的量来计算电解产物的量即可解答;
D.23Na37Cl中质子数和中子数分别是28和32.
解答 解:A.食用加碘盐可预防碘缺乏症,加碘盐中加的含碘物质是碘酸钾,故A错误;
B.电解质是化合物,NaCl溶液是混合物,不属于电解质,故B错误;
C.得到23g金属钠,则需要电解58.5g熔融的NaCl,能产生0.5mol×22.4L/mol=11.2L氯气(标准状况),而不是22.4L氯气,故C错误;
D.23Na37Cl中质子数和中子数分别是28和32,所以质子数和中子数之比是7:8,故D正确;
故选D.
点评 本题考查较为综合,涉及物质的量的计算、强弱电解质判断、原子构成等知识,题目难度不大,注意掌握强弱电解质的概念及判断方法,明确质量数与质子数、中子数的关系,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20. 在一固定容积的密闭容器中,进行如下反应:CO+H2O(g)?CO2+H2.其化学平衡常数K与温度T的关系如表:
在一固定容积的密闭容器中,进行如下反应:CO+H2O(g)?CO2+H2.其化学平衡常数K与温度T的关系如表:
回答下列问题:
(1)该反应的正反应为放(填“吸”或“放”)热反应.
(2)判断该反应到达平衡的依据是BCF(填字母代号)
A.容器内压强不变 B.混合气体中[CO]不变
C.V正(H2)=V逆(H2O) D.[CO]=[CO2]
E.K值不变 F.[CO]/[H2O]不变
(3)若容器的体积固定为10L,在容器中通入一定量的CO和H2O(g),并在T1℃时发生反应.
①CO和H2O的浓度变化如图所示,则在0-4min内正反应的平均反应速率为v(CO)0.03mol•L-1•min-1.
②此反应的温度等于850℃(填“大于”,“小于”或“等于”).
③图中6-7min浓度发生变化的原因可能是BE
A.只充入H2O(g) B.只升高温度
C.只使用催化剂 D.只充入惰性气体
E.只充入CO2
(4)850℃时,起始浓度[CO]=a mol/L,[H2O]=b mol/L,平衡时[H2]=c mol/L.则:
①a、b、c之间的关系是c2=(a-c)(b-c)或c=$\frac{ab}{a+b}$.
②当a=b时,a=2c.
 在一固定容积的密闭容器中,进行如下反应:CO+H2O(g)?CO2+H2.其化学平衡常数K与温度T的关系如表:
在一固定容积的密闭容器中,进行如下反应:CO+H2O(g)?CO2+H2.其化学平衡常数K与温度T的关系如表:| T(℃) | 700 | 800 | 850 | 1000 | 1200 |
| K | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的正反应为放(填“吸”或“放”)热反应.
(2)判断该反应到达平衡的依据是BCF(填字母代号)
A.容器内压强不变 B.混合气体中[CO]不变
C.V正(H2)=V逆(H2O) D.[CO]=[CO2]
E.K值不变 F.[CO]/[H2O]不变
(3)若容器的体积固定为10L,在容器中通入一定量的CO和H2O(g),并在T1℃时发生反应.
①CO和H2O的浓度变化如图所示,则在0-4min内正反应的平均反应速率为v(CO)0.03mol•L-1•min-1.
②此反应的温度等于850℃(填“大于”,“小于”或“等于”).
③图中6-7min浓度发生变化的原因可能是BE
A.只充入H2O(g) B.只升高温度
C.只使用催化剂 D.只充入惰性气体
E.只充入CO2
(4)850℃时,起始浓度[CO]=a mol/L,[H2O]=b mol/L,平衡时[H2]=c mol/L.则:
①a、b、c之间的关系是c2=(a-c)(b-c)或c=$\frac{ab}{a+b}$.
②当a=b时,a=2c.
7.常温下的下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A. | 10mL pH=13的氨水与10mL pH=l的盐酸混合:c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | l0 mL0.1 mol/L NH4Cl溶液与5mL 0.2mol/LNaOH溶液混合:c(Cl-)=c(Na+)>c(OH-)>(H+) | |
| C. | 10 mL 0.1 mol/L CH3COOH溶液与10 mL pH=13的NaOH溶液混合:c(CH3COO-)=c(Na+)>c(OH-)>c(H+) | |
| D. | l0 mL 0.5mol/L CH3COONa溶液与6mL pH=0的盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
1. 某学生用0.100 0mol/L的NaOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.100 0mol/L的NaOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
A.量取25.00mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准NaOH溶液注入碱式滴定管至刻度线0以上2cm~3cm;
E.调节液面至“0”或“0”以下刻度并记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记滴定管液面的刻度.
据此实验完成填空:
(1)正确操作步骤的顺序是B、D、C、E、A、F(用序号字母填写).
(2)上述B步骤操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(3)上述A步骤操作之前,先用待测溶液润洗锥形瓶,则对滴定结果的影响是偏高.
(4)判断到达滴定终点的实验现象是滴入最后一滴NaOH溶液,溶液由无色变为浅红色,且在半分钟内不褪色.
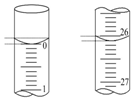
(5)若滴定开始和结束时,酸式滴定管中的液面如图所示:则起始读数为0.00mL,终点读数为26.10mL.
(6)某学生根据三次实验分别记录有关数据如上:请选用其中合理的数据列式计算该盐酸溶液的物质的量浓度:c(HCl)=0.1044mol/L.
 某学生用0.100 0mol/L的NaOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:
某学生用0.100 0mol/L的NaOH标准溶液滴定未知浓度的盐酸,其操作可分为如下几步:A.量取25.00mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准NaOH溶液注入碱式滴定管至刻度线0以上2cm~3cm;
E.调节液面至“0”或“0”以下刻度并记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记滴定管液面的刻度.
据此实验完成填空:
(1)正确操作步骤的顺序是B、D、C、E、A、F(用序号字母填写).
(2)上述B步骤操作的目的是防止滴定管内壁附着的水将标准溶液稀释而带来误差.
(3)上述A步骤操作之前,先用待测溶液润洗锥形瓶,则对滴定结果的影响是偏高.
| 滴定 次数 | 盐酸溶液/mL | 0.100 0mol•L-1NaOH的体积(mL) | ||
| 滴定前 | 滴定 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(5)若滴定开始和结束时,酸式滴定管中的液面如图所示:则起始读数为0.00mL,终点读数为26.10mL.
(6)某学生根据三次实验分别记录有关数据如上:请选用其中合理的数据列式计算该盐酸溶液的物质的量浓度:c(HCl)=0.1044mol/L.