题目内容
14.已知有以下物质相互转化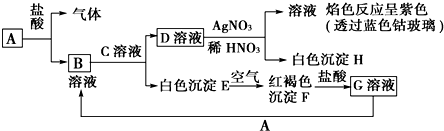
试回答:
(1)写出各物质的化学式:AFe,BFeCl2,CKOH,DKCl.
(2)向G溶液中滴加KSCN溶液的实验现象是溶液为血红色.
(3)向G溶液加入A的有关离子反应方程式2Fe3++Fe=3Fe2+.
(4)写出E到F的化学方程式:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
分析 由转化关系可知,白色沉淀E在空气中氧化生成红褐色沉淀F,则E为Fe(OH)2,F为Fe(OH)3,G为FeCl3,A与盐酸反应生成B和氢气,G与A反应生成B,则B为FeCl2,A为Fe,D与硝酸银反应生成白色沉淀H为AgCl,由焰色反应为紫色可知,溶液含钾离子,D为KCl,则C为KOH,以此来解答.
解答 解:由转化关系可知,白色沉淀E在空气中氧化生成红褐色沉淀F,则E为Fe(OH)2,F为Fe(OH)3,G为FeCl3,A与盐酸反应生成B和氢气,G与A反应生成B,则B为FeCl2,A为Fe,D与硝酸银反应生成白色沉淀H为AgCl,由焰色反应为紫色可知,溶液含钾离子,D为KCl,则C为KOH,
(1)由上述分析可知,A为Fe,B为FeCl2,C为KOH,D为KCl,故答案为:Fe;FeCl2;KOH;KCl;
(2)G为FeCl3,向G溶液中滴加KSCN溶液的实验现象是溶液为血红色,故答案为:溶液为血红色;
(3)向G溶液加入A的有关离子反应方程式为2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(4)白色沉淀E在空气中放置反应的化学方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评 本题考查无机物的推断,为高频考点,明确红褐色沉淀F为氢氧化铁为推断的突破口,把握铁及其化合物的性质、相互转化反应为解答的关键,侧重分析与推断能力的考查,注意元素化合物知识的综合应用,题目难度中等.

练习册系列答案
相关题目
4.研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是( )
| A. | 负极反应式:Ag-e-═Ag+ | |
| B. | 每生成1mol Na2Mn5O10,MnO2在正极得到2mol电子 | |
| C. | Na+不断向“水”电池的负极移动 | |
| D. | AgCl是还原产物 |
2.下列羧酸在常温下呈固态的是( )
| A. | CH3CH2COOH | B. | HCOOH | C. | C17H35COOH | D. | H17H33COOH |
9.2SO2(g)+O2(g)$?_{△}^{催化剂}$2SO3(g)是制备硫酸过程中的一步重要反应,下列叙述正确的是( )
| A. | 催化剂不会改变该反应的逆反应速率 | |
| B. | 增大SO2(g)的浓度,逆反应速率会减小 | |
| C. | 该反应是放热反应,降低温度将缩短反应达到平衡的时间 | |
| D. | 在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=$\frac{{c}_{2}-{c}_{1}}{{t}_{2}-{t}_{1}}$ |
19.下列关于钠的叙述错误的是( )
| A. | 钠在常温下很容易被氧化 | B. | 钠在空气中燃烧生成Na2O | ||
| C. | 钠燃烧时发出黄色的火焰 | D. | 钠的密度比水小,熔点低于100℃ |
4.3.15g镁铝合金完全溶于稀硝酸.若反应中硝酸被还原只产生2.24L(标准状况下)NO气体,在反应后的溶液中加认足量1mo1•L-1的NaOH溶液.生成沉淀的质量为( )
| A. | 8.7g | B. | 3.15g | C. | 4.35g | D. | 4.0g |
