题目内容
8.下列物质中属于电解质是( )| A. | 液态溴化氢 | B. | 蔗糖 | C. | 铝 | D. | 硝酸溶液 |
分析 在水溶液或者熔融状态下能够导电的化合物是电解质,在水溶液和熔融状态下都不导电的化合物是非电解质,电解质必须本身能够电离,单质和化合物既不是电解质也不是非电解质.
解答 解:A.液态溴化氢溶于水能够导电,属于电解质,故A正确;
B.蔗糖在水溶液和熔融状态下都不导电的化合物是非电解质,故B错误;
C.铝是单质,既不是电解质也不是非电解质,故C错误;
D.硝酸溶液是混合物,既不是电解质也不是非电解质,故D错误;
故选:A.
点评 本题考查了电解质、非电解质的判断,明确电解质、非电解质概念是解题关键,注意电解质必须本身能够电离,单质和化合物既不是电解质也不是非电解质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.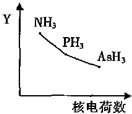 氮族元素氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的是( )
氮族元素氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的是( )
 氮族元素氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的是( )
氮族元素氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如图所示,则Y轴可表示的是( )| A. | 相对分子质量 | B. | 稳定性 | C. | 沸点 | D. | R-H键长 |
19.在日常生活和生产过程中化学有着重要的应用,下列有关说法正确的是( )
| A. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,也称为可入肺颗粒物,分散在空气中不可能形成胶体 | |
| B. | 生活中常见的石英玻璃、普通玻璃、钢化玻璃都属于硅酸盐产品 | |
| C. | 食品添加剂对人体均有益,可随意使用 | |
| D. | 洪涝、地震灾区灾后可用石灰消毒,是利用石灰可使蛋白质变性的性质 |
16.下列鉴别方法不能达到实验目的是( )
| A. | 用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体 | |
| B. | 用KOH溶液鉴别NH4Cl、AlCl3、MgSO4、FeCl3四种溶液 | |
| C. | 用盐酸溶液鉴别Na2CO3溶液和Na2SiO3溶液 | |
| D. | 用BaCl2溶液鉴别AgNO3和Na2SO4 |
13.下列有关化学用语表示正确的是( )
| A. | -CHO的电子式: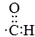 | B. | 乙醇的分子式:CH3CH2OH | ||
| C. | 乙烯的结构简式为:CH2CH2 | D. | 丙烷分子的球棍模型: |
20.一定能在下列溶液中大量共存的离子组是( )
| A. | PH=12的溶液:NH4+、Na+、Cl-、HCO3- | |
| B. | 能使pH试纸变红色的溶液:Na+、Al3+、NO3-、SO42- | |
| C. | 含有大量Fe3+的溶液:SCN-、I-、K+、Br- | |
| D. | 澄清透明的无色溶液:ClO-、MnO4-、Al3+、SO42- |
17.下列化学用语正确的是( )
| A. | 硅的原子结构示意图: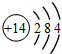 | B. | 乙烯分子比例模型: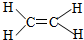 | ||
| C. | 次氯酸分子的电子式: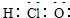 | D. | 乙酸分子的结构简式:C2H4O2 |
18.工业上常用浓氨水检验氯气管道,其反应为:3Cl2+8NH3═6NH4Cl+N2,利用该反应中产物白烟这一现象来判断管道是否漏气,关于该反应的说法不正确的是( )
| A. | 氧化剂是Cl2 | |
| B. | 氧化剂与还原剂的物质的量之比为3:8 | |
| C. | 每生成1molN2,转移3mol电子 | |
| D. | 被氧化与未被氧化的NH3物质的量之比为1:3 |