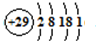题目内容
铜单质及其化合物在很多领域有重要的用途,如超细铜粉可应用于导电材料、催化剂等领域中。超细铜粉的某制备方法如下:

(1)[Cu(NH3)4]SO4中,N、O、S三种元素的第一电离能从大到小的顺序为: 。
(2) SO42-中硫原子的杂化轨道类型是 :写出一种与SO42-互为等电子体的分子 。
(3)某反应在超细铜粉做催化剂作用下生成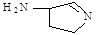 ,则分子中 σ 键与 π 键之比为
,则分子中 σ 键与 π 键之比为
(4)该化合物[Cu(NH3)4]SO4中存在的化学键类型有 。(填字母)
A.离子键 B.金属键 C.配位键 D.非极性键 E.极性键
(5)NH4CuSO3中的金属阳离子的核外电子排布式为 。
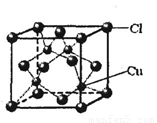
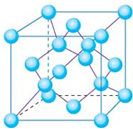
(6)铜的某氯化物的晶胞结构如右图所示,该化合物的化学式为 。
(1)N>O>S (2)SP3杂化,CCl4 (3)14∶1
(4)ACE(选对两个得1分,只要选错得0分)
(5)1S22S22P63S23P63d10或[Ar] 3d10 (6)CuCl
【解析】
试题分析:⑴ 元素周期律中,同一周期元素的第一电离能随着原子序数的增大而增大,但第ⅡA和第ⅢA、第ⅤA和第ⅥA互换,同一主族元素的第一电离能随着原子序数的增大而减小,所以其第一电离能大小为 N>O>S.故答案为:N>O>S
⑵SO42-离子中价层电子对数为4+1/2(6+2―4×2)=4,孤电子对数为0,SP3杂化,所以是正四面体体型.原子个数相等且价电子数相等的微粒为等电子体,与SO42-互为等电子体的分子如:CCl4 。
故答案为:SP3杂化,CCl4
(3)共价单键是σ键,共价双键中一个是σ键一个是π键,该物质中含有14个σ键1个是π键,所以分子中σ键与π键之比为14:1,故答案为:14:1;
(4)[Cu (NH3 )4]SO4中硫酸根离子和[Cu(NH3)4]2+存在离子键,N原子和铜原子之间存在配位键,NH3中H和N之间存在共价键,所以[Cu(NH3)4]SO4中所含的化学键有共价键、离子键、配位键,故选ACE;
(5)NH4CuSO3中的金属阳离子是Cu+,基态Cu+核外有28个电子,根据构造原理知其核外电子排布式为:1S22S22P63S23P63d10或[Ar]3d10,故答案为:1S22S22P63S23P63d10或[Ar]3d10;
(6)该晶胞中铜原子个数是4,氯原子个数=8×1/8+6×1/2=4,所以其化学式为:CuCl,故答案为:CuCl.
考点:化学键;原子核外电子排布;元素电离能、电负性的含义及应用;判断简单分子或离子的构型;离子晶体;原子轨道杂化方式及杂化类型判断.

 碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.