题目内容
16.400K,101.3kPa时,1.5L某烃蒸气能在aL氧气中完全燃烧,体积增大至(a+3)L(相同条件下).若a=8L时,该烃可能的分子式是( )| A. | CH4 | B. | C2H6 | C. | C4H8 | D. | C3H8 |
分析 400K水为气体,设烃为CxHy,由CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,利用气体体积差量确定y值,然后结合a=8L时1.5(x+$\frac{y}{4}$)≤8,据此确定该烃的分子式.
解答 设烃的分子式为CxHy,则:
CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O 气体体积差量△V
1 (x+$\frac{y}{2}$-x-$\frac{y}{4}$-1)
1.5L (a+3-a-1.5)L
解得:y=8;
即该烃的分子式满足:CxH8,
若a=8时,由于该烃完全燃烧,则:1.5(x+$\frac{y}{4}$)≤8,解得:x≤$\frac{10}{3}$,
根据以上分析可知,满足条件的为D,
故选D.
点评 本题考查了有机物分子式确定的计算,题目难度中等,明确发生反应原理为解答关键,注意掌握差量法、讨论法在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
7. 在常温下,用0.1000mol/L的盐酸滴定25mL 0.1000mol/L Na2CO3溶液,所得滴定曲线如图所示.下列有关滴定过程中溶液相关微粒浓度间的关系不正确的是( )
在常温下,用0.1000mol/L的盐酸滴定25mL 0.1000mol/L Na2CO3溶液,所得滴定曲线如图所示.下列有关滴定过程中溶液相关微粒浓度间的关系不正确的是( )
 在常温下,用0.1000mol/L的盐酸滴定25mL 0.1000mol/L Na2CO3溶液,所得滴定曲线如图所示.下列有关滴定过程中溶液相关微粒浓度间的关系不正确的是( )
在常温下,用0.1000mol/L的盐酸滴定25mL 0.1000mol/L Na2CO3溶液,所得滴定曲线如图所示.下列有关滴定过程中溶液相关微粒浓度间的关系不正确的是( )| A. | a点:c( HCO3-)>c(Cl-)>c(CO32-) | |
| B. | b点:c(Na+)+c(H+)=c(Cl一)+c(HCO3-)+c(CO32-)+c(OH -) | |
| C. | c点:c(OH -)+c(CO32-)=c(H+)+c(H2CO3) | |
| D. | d点:c(Cl-)=c(Na+) |
11.下列微粒中只有氧化性的是( )
①S2- ②Fe2+ ③Fe3+ ④S ⑤Na+ ⑥HClO4⑦Mg.
①S2- ②Fe2+ ③Fe3+ ④S ⑤Na+ ⑥HClO4⑦Mg.
| A. | ①⑦ | B. | ②④ | C. | ③⑤⑥ | D. | ②④⑤⑥ |
1.常温下,将pH=2的盐酸与pH=2的醋酸溶液等体积混合后,溶液的pH( )
| A. | =2 | B. | >2 | C. | <2 | D. | 无法确定 |
8.下列各组中的物质,能在溶液中大量共存的是( )
| A. | KNO3 NaCl NaOH | B. | KOH Na2CO3 HCl | ||
| C. | KNO3 NaOH FeCl3 | D. | AgNO3 BaCl2 HNO3 |
17.短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是( )
| A. | W、Y、Z的非金属性强弱顺序一定是Z>Y>W | |
| B. | W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z | |
| C. | W和Z形成的物质中只含离子键 | |
| D. | 由Y形成的氢化物中可能是H2Y或YH3、YH4 |
18.聚合氯化铝(PAC)是常用于水质净化的无机高分子混凝剂,其化学式可表示为[Al2(OH)nCl6-n]m(n<6,m为聚合度).PAC常用高温活化后的高岭土(主要化学组成为Al2O3、SiO2、Fe2O3)进行制备,工艺流程如图1所示:
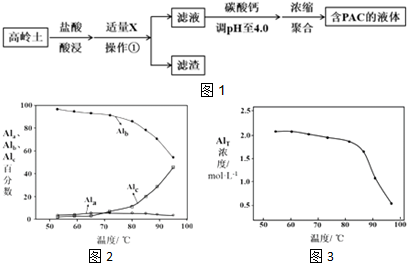
(1)盐酸酸浸所涉及反应的离子方程式是6H++Al2O3═2Al3++3H2O、6H++Fe2O3═2Fe3++3H2O.
(2)已知:生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol•L-1
根据表中数据解释加入X的主要目的:调节溶液pH至Fe3+完全沉淀,滤渣中主要含有物质的化学式是Fe(OH)3、SiO2.
(3)已知:生成液体PAC的反应为2Al3++m(6-n) Cl-+mn H2O?[Al2(OH)nCl6-n]m+mn H+.用碳酸钙调节溶液的pH时,要严控pH的大小,pH偏小或偏大液体PAC的产率都会降低.请解释pH偏小液体PAC产率降低的原因:pH偏小时,抑制平衡2Al3++m(6-n)Cl-+mnH2O?[Al2(OH)nCl6-n]m+mnH+正向移动生成PAC.
(4)浓缩聚合得到含PAC的液体中铝的各种形态主要包括:
Ala--Al3+单体形态铝
Alb--[Al2(OH)nCl6-n]m聚合形态铝
Alc--Al(OH)3胶体形态
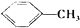
图2为Al各形态百分数随温度变化的曲线;图3为含PAC的液体中铝的总浓度AlT随温度变化的曲线.
①50-90℃之间制备的液体PAC中,聚合形态铝含量最多.
②当T>80℃时,AlT明显降低的原因是温度升高,导致液体PAC向Al(OH)3沉淀转化.

(1)盐酸酸浸所涉及反应的离子方程式是6H++Al2O3═2Al3++3H2O、6H++Fe2O3═2Fe3++3H2O.
(2)已知:生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 1.5 |
| 完全沉淀时 | 4.7 | 2.8 |
根据表中数据解释加入X的主要目的:调节溶液pH至Fe3+完全沉淀,滤渣中主要含有物质的化学式是Fe(OH)3、SiO2.
(3)已知:生成液体PAC的反应为2Al3++m(6-n) Cl-+mn H2O?[Al2(OH)nCl6-n]m+mn H+.用碳酸钙调节溶液的pH时,要严控pH的大小,pH偏小或偏大液体PAC的产率都会降低.请解释pH偏小液体PAC产率降低的原因:pH偏小时,抑制平衡2Al3++m(6-n)Cl-+mnH2O?[Al2(OH)nCl6-n]m+mnH+正向移动生成PAC.
(4)浓缩聚合得到含PAC的液体中铝的各种形态主要包括:
Ala--Al3+单体形态铝
Alb--[Al2(OH)nCl6-n]m聚合形态铝
Alc--Al(OH)3胶体形态
图2为Al各形态百分数随温度变化的曲线;图3为含PAC的液体中铝的总浓度AlT随温度变化的曲线.
①50-90℃之间制备的液体PAC中,聚合形态铝含量最多.
②当T>80℃时,AlT明显降低的原因是温度升高,导致液体PAC向Al(OH)3沉淀转化.

 $→_{△}^{MnO_{4}/H+}$
$→_{△}^{MnO_{4}/H+}$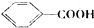
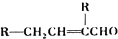
 .
. .
. (写出其中一种结构简式)
(写出其中一种结构简式) .
.

 ;
;