题目内容
常温下,将Na2CO3和NaHCO3混合物〔
=a a≤3〕溶于水制得稀溶液,下列有关该溶液中微粒的物质的量浓度关系正确的是( )
| n(Na2CO3) |
| n(NaHCO3) |
| A、a=1则c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| B、a=2则c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| C、a为任意值时,则c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-) |
| D、a=0则c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:A.a=1时,碳酸根离子的水解程度大于碳酸氢根离子,则溶液中c(CO32-)<c(HCO3-);
B.
=2,碳酸钠的物质的量为碳酸氢钠的2倍,根据混合液中电荷守恒、物料守恒判断;
C.溶液中一定满足电荷守恒,根据混合液中的电荷守恒判断;
D.a=0时,碳酸钠的物质的量为0,该溶液为碳酸氢钠溶液,根据碳酸氢钠溶液中的离子浓度大小判断.
B.
| n(Na2CO3) |
| n(NaHCO3) |
C.溶液中一定满足电荷守恒,根据混合液中的电荷守恒判断;
D.a=0时,碳酸钠的物质的量为0,该溶液为碳酸氢钠溶液,根据碳酸氢钠溶液中的离子浓度大小判断.
解答:
解:A.a=1,碳酸氢钠与碳酸钠的物质的量相等,由于碳酸根离子的水解程度大于碳酸氢根离子,则c(CO32-)<c(HCO3-),溶液中离子浓度大小关系为:c(HCO3-)>c(CO32-)>c(OH-)>c(H+),故A错误;
B.溶液中存在电荷守恒c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),存在物料守恒3c(Na+)=5c(CO32-)+5c(HCO3-)+5c(H2CO3),则3c(OH-)=3c(H+)+2c(HCO3-)+5c(H2CO3)+2c(CO32-),故B错误;
C.a为任意值时,溶液中一定满足电荷守恒,根据电荷守恒可得:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故C正确;
D..
=a=0时,碳酸钠的物质的量为0,该溶液为碳酸氢钠溶液,碳酸氢钠溶液中,碳酸氢根离子部分水解,溶液显示碱性,由于碳酸氢根离子的水解程度远远大于其电离程度,则c(OH-)>c(H+)>c(CO32-),所以溶液中离子浓度大小为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+)>c(CO32-),故D错误;
故选C.
B.溶液中存在电荷守恒c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),存在物料守恒3c(Na+)=5c(CO32-)+5c(HCO3-)+5c(H2CO3),则3c(OH-)=3c(H+)+2c(HCO3-)+5c(H2CO3)+2c(CO32-),故B错误;
C.a为任意值时,溶液中一定满足电荷守恒,根据电荷守恒可得:c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-),故C正确;
D..
| n(Na2CO3) |
| n(NaHCO3) |
故选C.
点评:本题考查了溶液中离子浓度大小比较,题目难度中等,注意掌握判断溶液中离子浓度大小比较的方法,明确电解原理及其应用方法,还要注意电荷守恒、物料守恒的含义及其应用,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
将0.2mol?L-1 NaHCO3溶液与0.1mol?L-1 KOH溶液等体积混合,下列关系正确的是( )
| A、2c(K+)=c(HCO3-)+2c(CO32-)+c(H2CO3) |
| B、c(Na+)>c(K+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| C、c(OH-)+c(CO32-)=c(H+)+c(H2CO3)+0.1mol?L-1 |
| D、3c(K+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
下列四组物质的水溶液,仅用一种试剂不能完成组内各种溶液的鉴别的是( )
| A、Na2CO3、NaCl、AgNO3 |
| B、Na2SO4、NaOH、HCl |
| C、CuSO4、Na2SO4、NaNO3 |
| D、K2SO4、KNO3、KCl |
某链状有机物分子中含有m个-CH3,n个-CH2-,a个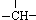 ,其余为-NH2,则-NH2的数目可能是( )
,其余为-NH2,则-NH2的数目可能是( )
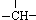 ,其余为-NH2,则-NH2的数目可能是( )
,其余为-NH2,则-NH2的数目可能是( )| A、2n+3-m |
| B、a+2-m |
| C、n+m+a |
| D、a+2n+2-m |
Cu2+、Fe2+、Fe3+生成沉淀的pH如下:则在pH=4的溶液中能够大量共存的离子组是( )
| 物质 | Cu(OH)2 | Fe (OH)2 | Fe (OH)3 |
| 开始沉淀pH | 4.2 | 5.8 | 1.2 |
| 完全沉淀pH | 6.7 | 8.3 | 3.2 |
| A、Fe3+、Cu2+、Cl-、NO3- |
| B、Fe2+、K+、SO42-、NO3- |
| C、Cu2+、Na+、CO32-、SO42- |
| D、Fe2+、K+、SO42-、Cl- |
下列事实不能用勒夏特列原理解释的是( )
| A、黄绿色的氯水光照后颜色变浅 |
| B、由H2、I2蒸气、HI组成的平衡体系加压后颜色变深 |
| C、温度过高对合成氨不利 |
| D、溴水中有平衡:Br2+H2O?HBr+HBrO,当加入AgNO3溶液后,溶液颜色变浅 |
下列各组溶液中,c(NO3-) 与200mL 0.2mol/L NaNO3溶液中的c(NO3-) 相同的是( )
| A、100mL 0.4mol/L KNO3溶液 |
| B、100mL 0.2mol/L Cu(NO3)2溶液 |
| C、200mL 0.1mol/L Fe(NO3)2溶液 |
| D、400mL 0.1mol/L Al(NO3)3溶液 |
