题目内容
书写下列反应的热化学方程式:
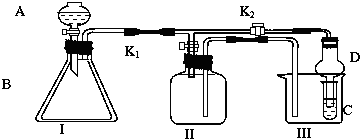
Ⅰ.根据下列图示,写出反应的热化学方程式:

(1)
(2)
Ⅱ.写出下列反应的热化学方程式:
(3)1mol N2(气态)与适量O2(气态)起反应,生成NO(气态)需吸收68kJ的热量
(4)卫星发射时可用肼(N2H4)为燃料,1mol N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出534kJ的热量
Ⅲ.图(3)是N2与H2反应过程中能量变化的曲线图:
(5)该反应的热化学方程式为 .
Ⅰ.根据下列图示,写出反应的热化学方程式:

(1)
(2)
Ⅱ.写出下列反应的热化学方程式:
(3)1mol N2(气态)与适量O2(气态)起反应,生成NO(气态)需吸收68kJ的热量
(4)卫星发射时可用肼(N2H4)为燃料,1mol N2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出534kJ的热量
Ⅲ.图(3)是N2与H2反应过程中能量变化的曲线图:
(5)该反应的热化学方程式为
考点:热化学方程式,有关反应热的计算
专题:化学反应中的能量变化
分析:Ⅰ、(1)(2)根据热化学方程式的书写方法可知,方程式反写,反应热符合相反,并注意标明物质的聚集状态来解答.
Ⅱ、(3)书写热化学方程式除了要遵循书写化学方程式的要求外,还应注意必须注明各反应物、生成物的状态(s、l、g、aq)等要求,根据热化学方程式的书写方法解答;
(4)放热时焓变值为负值,根据热化学方程式的书写方法解答;
(5)依据热化学方程式的书写原则,标注物质的聚集状态和反应的热效应,结合断键吸收热量,形成化学键放出热量计算反应的焓变,△H=放出的能量-吸收的能量分析;
Ⅱ、(3)书写热化学方程式除了要遵循书写化学方程式的要求外,还应注意必须注明各反应物、生成物的状态(s、l、g、aq)等要求,根据热化学方程式的书写方法解答;
(4)放热时焓变值为负值,根据热化学方程式的书写方法解答;
(5)依据热化学方程式的书写原则,标注物质的聚集状态和反应的热效应,结合断键吸收热量,形成化学键放出热量计算反应的焓变,△H=放出的能量-吸收的能量分析;
解答:
解:Ⅰ、根据热化学方程式的书写方法可知,方程式反写,反应热符合相反,并注意标明物质的聚集状态,根据图象写出热化学方程为:
(1)CO(g)+2H2O(g)═CO2(g)+H2(g)△H=-41 kJ?mol-1;
故答案为:CO(g)+2H2O(g)═CO2(g)+H2(g)△H=-41 kJ?mol-1 ;
(2)CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41 kJ?mol-1;
故答案为:CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41 kJ?mol-1;
Ⅱ、(3)1mol N2 (g)与适量O2(g)起反应,生成NO2(g),吸收68kJ热量,反应吸热时焓变值为正值,所以该反应的热化学方程式为N2(g)+2O2(g)=2NO2(g)△H=+68kJ?mol-1,
故答案为:N2(g)+2O2(g)=2NO2(g)△H=+68kJ?mol-1;
(4)1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(g),放出534kJ热量放热时焓变值为负值,所以该反应的热化学方程式为N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-622kJ?mol-l,
故答案为:N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ?mol-l;
(5)热化学方程式必须标注物质的聚集状态反应的焓变,分析图象反应焓变=508KJ/mol-600KJ/mol=-92KJ/mol,该反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g),△H=-92kJ?mol-1;
故答案为:N2(g)+3H2(g)?2NH3(g),△H=-92kJ?mol-1;
(1)CO(g)+2H2O(g)═CO2(g)+H2(g)△H=-41 kJ?mol-1;
故答案为:CO(g)+2H2O(g)═CO2(g)+H2(g)△H=-41 kJ?mol-1 ;
(2)CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41 kJ?mol-1;
故答案为:CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41 kJ?mol-1;
Ⅱ、(3)1mol N2 (g)与适量O2(g)起反应,生成NO2(g),吸收68kJ热量,反应吸热时焓变值为正值,所以该反应的热化学方程式为N2(g)+2O2(g)=2NO2(g)△H=+68kJ?mol-1,
故答案为:N2(g)+2O2(g)=2NO2(g)△H=+68kJ?mol-1;
(4)1mol N2H4(l)在O2(g)中燃烧,生成N2(g)和H2O(g),放出534kJ热量放热时焓变值为负值,所以该反应的热化学方程式为N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-622kJ?mol-l,
故答案为:N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-534kJ?mol-l;
(5)热化学方程式必须标注物质的聚集状态反应的焓变,分析图象反应焓变=508KJ/mol-600KJ/mol=-92KJ/mol,该反应的热化学方程式为:N2(g)+3H2(g)?2NH3(g),△H=-92kJ?mol-1;
故答案为:N2(g)+3H2(g)?2NH3(g),△H=-92kJ?mol-1;
点评:本题主要考查了热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,盖斯定律的运用.题目难度不大.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
某烃完全燃烧后,生成二氧化碳和水的物质的量之比为n:(n-1),此烃可能是( )
| A、烷烃 | B、单烯烃 |
| C、炔烃 | D、苯的同系物 |
0.1mol某单质跟足量的硫充分反应后,其质量增加1.6g.则组成这种单质的元素可能是( )
| A、Cu | B、Al | C、Zn | D、Fe |
我们每天都和化学变化打交道,以下说法没有化学变化的是( )
| A、吃进的食物一段时间被消化了 |
| B、课外活动时,呼吸作用增强 |
| C、水放进冰箱里一段时间后结成冰 |
| D、人体吸收各种氨基酸后合成各种蛋白质 |
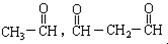 ,试写出该烃的结构简式.
,试写出该烃的结构简式.