题目内容
 H、C、N、O、Na、Fe、Cu是常见的七种元素.
H、C、N、O、Na、Fe、Cu是常见的七种元素.(1)N、Na+、Fe3+、Cu2+四种微粒基态的核外电子排布式中未成对电子数最多的是
(2)根据价层电子对互斥理论判断下列分子或离子中空间构型是V形的是
a.H3O+ b.H2O c.NO2+ d.NO2-
(3)分子(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子最外层均满足8电子稳定结构,其结构式为
(4)O和Na形成的一种只含有离子键的离子化合物,其晶胞结构如图,该离子化合物的化学式为
已知该晶胞的密度为ρg/cm3,阿伏加德罗常数为NA,求晶胞边长a=
考点:晶胞的计算,原子核外电子排布,判断简单分子或离子的构型
专题:
分析:(1)在N、Na+、Fe3+、Cu2+四种微粒基态的核外电子排布式中,未成对电子数依次是3、0、5、1,据此可作判断;
(2)根据分子或离子中中心原子价层电子对数和孤电子对数判断;
(3)分子(CN)2中碳原子按sp杂化,碳碳之间是单键,碳氮之间是参键,碳氮参键中有两个π键,据此判断;
(4)利用均摊法确定晶胞中含有离子个数,进而确定化学式,根据ρ=
求得晶胞体积,再求得晶胞边长;
(2)根据分子或离子中中心原子价层电子对数和孤电子对数判断;
(3)分子(CN)2中碳原子按sp杂化,碳碳之间是单键,碳氮之间是参键,碳氮参键中有两个π键,据此判断;
(4)利用均摊法确定晶胞中含有离子个数,进而确定化学式,根据ρ=
| m |
| V |
解答:
解:(1)在N、Na+、Fe3+、Cu2+四种微粒基态的核外电子排布式中,未成对电子数依次是3、0、5、1,所以未成对电子数最多的是Fe3+,
故答案为:Fe3+;
(2)H3O+中中心原子O的价层电子对数为
=4,孤电子对数为1,所以空间构型是三角锥形;H2O中中心原子O的价层电子对数为
=4,孤电子对数为2,所以空间构型是V形;NO2+中中心原子N的价层电子对数为
=2,孤电子对数为0,所以空间构型是直线形;NO2-中中心原子N的价层电子对数为
=3,孤电子对数为1,所以空间构型是V形,
故选bd;
(3)分子(CN)2中碳原子按sp杂化,碳碳之间是单键,碳氮之间是参键,其结构式为N≡C-C≡N,碳氮参键中有两个π键,所以1个分子中含有4个π键,
故答案为:N≡C-C≡N;4;
(4)根据晶胞结构图,利用均摊法可知,晶胞中含有氧离子个数为8×
+6×
=4,含有钠离子个数为8,所以化学式为Na2O,根据ρ=
可知晶胞体积V=
cm3=
cm3=
cm3,所以晶胞边长=
,
故答案为:Na2O;
;
故答案为:Fe3+;
(2)H3O+中中心原子O的价层电子对数为
| 6+3-1 |
| 2 |
| 6+2 |
| 2 |
| 5-1 |
| 2 |
| 5+1 |
| 2 |
故选bd;
(3)分子(CN)2中碳原子按sp杂化,碳碳之间是单键,碳氮之间是参键,其结构式为N≡C-C≡N,碳氮参键中有两个π键,所以1个分子中含有4个π键,
故答案为:N≡C-C≡N;4;
(4)根据晶胞结构图,利用均摊法可知,晶胞中含有氧离子个数为8×
| 1 |
| 8 |
| 1 |
| 2 |
| m |
| V |
| m |
| ρ |
| ||
| ρ |
| 248 |
| ρ?NA |
| 3 |
| ||
故答案为:Na2O;
| 3 |
| ||
点评:本题主要考查了核外电子排布、离子分子空间构型、化学键、晶胞的计算等知识点,中等难度,注意基础知识的全面掌握.

练习册系列答案
相关题目
实验室需用到480mL 0.1mol/L 的稀盐酸,拟用量筒取用5mol/L的浓盐酸在容量瓶中进行配制.下列有关说法正确的是( )
| A、应量取的浓盐酸的体积是9.6mL |
| B、若开始时洁净的容量瓶中有少许蒸馏水,对实验没有影响 |
| C、量取浓盐酸时,仰视量筒将使所配溶液的浓度偏低 |
| D、定容摇匀后,发现液面低于刻度线,应立即加少量蒸馏水补齐 |
下列各组离子在指定的溶液中能大量共存的是( )
| A、强酸性溶液中:Na+,Fe2+,Cl-,ClO- |
| B、加入Al能放出的H2溶液中:Cl-,HCO3-,NO3-,NH4+ |
| C、在由水电离出的c(OH-)=10-13mol?L-1的溶液中:Fe2+,Al3+,NO3-,Cl- |
| D、pH=11的溶液中:CO32-,Na+,[Al(OH)4]-,NO3- |
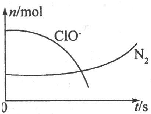 某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中N2、ClO-的物质的量随时间变化的曲线如右图所示.下列判断不正确的是( )
某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒.其中N2、ClO-的物质的量随时间变化的曲线如右图所示.下列判断不正确的是( )| A、该反应的氧化剂是ClO- |
| B、消耗1 mol还原剂,转移3 mol电子 |
| C、氧化剂与还原剂的物质的量之比为2:3 |
| D、反应后溶液的酸性明显增强 |
