题目内容
通过石油裂解可以获得乙烯,再以乙烯为原料还可以合成很多的化工产品,已知乙烯能发生以下转化:
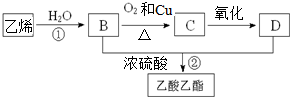
(1)乙烯的结构简式为: ;
(2)反应①的反应类型是 ;D所含官能团的名称为 ;
(3)写出以下反应的化学方程式:
① ;
② ;
(4)在实验室中获得的乙酸乙酯往往含有B、D,为提纯乙酸乙酯,加入的试剂以及分离操作方法是 、 ;
(5)假设反应②转化率是60%,其余反应的转化率都是100%,则用标准状况下4.48×105m3的乙烯,理论上最多能生产出乙酸乙酯 .

(1)乙烯的结构简式为:
(2)反应①的反应类型是
(3)写出以下反应的化学方程式:
①
②
(4)在实验室中获得的乙酸乙酯往往含有B、D,为提纯乙酸乙酯,加入的试剂以及分离操作方法是
(5)假设反应②转化率是60%,其余反应的转化率都是100%,则用标准状况下4.48×105m3的乙烯,理论上最多能生产出乙酸乙酯
考点:有机物的推断
专题:有机物的化学性质及推断
分析:C2H4与水发生加成反应生成B为CH3CH2OH,乙醇在Cu作催化剂条件下发生氧化反应生成C为CH3CHO,CH3CHO可进一步氧化物生成D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成CH3COOCH2CH3.
解答:
解:C2H4与水发生加成反应生成B为CH3CH2OH,乙醇在Cu作催化剂条件下发生氧化反应生成C为CH3CHO,CH3CHO可进一步氧化物生成D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成CH3COOCH2CH3,
(1)乙烯的结构简式为:CH2=CH2,故答案为:CH2=CH2;
(2)反应①是乙烯与水发生加成反应,D为CH3COOH,所含官能团的名称为羧基,
故答案为:加成反应;羧基;
(3)反应①的化学方程式为:CH2=CH2+H2O
CH3CH2OH;
反应②的化学方程式为:CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O,
故答案为:CH2=CH2+H2O
CH3CH2OH;CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O;
(4)在实验室中获得的乙酸乙酯往往含有乙醇、乙酸,为提纯乙酸乙酯,加入的饱和碳酸钠溶液,再进行分液分离,故答案为:饱和碳酸钠溶液;分液;
(5)由反应CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O可知乙醇与乙酸按1:1反应,故4.48×105m3乙烯有一半的用于生成乙醇,另一半用于生成乙酸,根据CH2=CH2~CH3CH2OH~CH3CHO~CH3COOH可知,n(CH3CH2OH)=n(CH3COOH)=
×
=1×107mol,生成乙酸乙酯的转化率为60%,故生成CH3COOCH2CH3的物质的量为1×107mol×60%,故乙酸乙酯的质量为:1×107mol×60%×88g/mol=528×106g=528吨,
故答案为:528吨.
(1)乙烯的结构简式为:CH2=CH2,故答案为:CH2=CH2;
(2)反应①是乙烯与水发生加成反应,D为CH3COOH,所含官能团的名称为羧基,
故答案为:加成反应;羧基;
(3)反应①的化学方程式为:CH2=CH2+H2O
| 一定条件 |
反应②的化学方程式为:CH3CH2OH+CH3COOH
| 浓硫酸 |
| △ |
故答案为:CH2=CH2+H2O
| 一定条件 |
| 浓硫酸 |
| △ |
(4)在实验室中获得的乙酸乙酯往往含有乙醇、乙酸,为提纯乙酸乙酯,加入的饱和碳酸钠溶液,再进行分液分离,故答案为:饱和碳酸钠溶液;分液;
(5)由反应CH3CH2OH+CH3COOH
| 浓硫酸 |
| △ |
| 4.48×108L |
| 22.4L/mol |
| 1 |
| 2 |
故答案为:528吨.
点评:本题考查有机物推断以及烯与醇、醛、羧酸之间的转化关系等,难度中等,(5)中计算为易错点,注意乙烯有一半的用于生成乙醇,另一半用于生成乙酸,利用C元素守恒计算更简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法正确的是( )
| A、在AgNO3溶液中依次滴加同浓度的NaCl、Na2S溶液,可证明KSP(AgCl)>KSP(Ag2S) |
| B、△S>0的反应在一定条件下不一定可以自发进行 |
| C、以Al作阳极,Fe作阴极,可以实现铁上镀铝 |
| D、工业合成SO3不采用高压是因为增大压强对SO2的转化率影响不大 |
下列有关物质性质、应用的说法中不正确的是( )
| A、Al2O3既能溶于NaOH溶液又能溶于HCl,说明Al2O3是两性氧化物 |
| B、浓硫酸能干燥SO2、NO2等气体,说明浓硫酸具有吸水性 |
| C、SO2气体具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 |
| D、石英的主要成分是SiO2 |
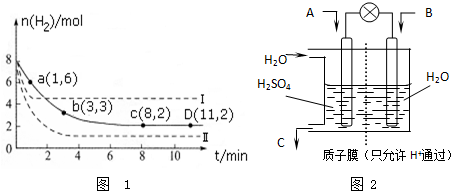
 如图中A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物.请回答下列问题:
如图中A、B、C、D、E均为有机化合物.已知:C能跟NaHCO3溶液发生反应,C和D的相对分子质量相等,且E为无支链的化合物.请回答下列问题: