题目内容
5.下列指定反应的离子方程式正确的是( )| A. | Fe3O4溶于足量稀HNO3:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| B. | NaHSO4溶液与Ba(OH)2溶液混合至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | K37ClO3与浓盐酸在加热条件下生成氯气:37ClO3-+6Cl-+6H+═37Cl-+3Cl2↑+3H2O | |
| D. | 4mol•L-1的NaAlO2溶液与7mol•L-1的盐酸等体积互相均匀混合:4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ |
分析 A.Fe3O4溶于足量稀HNO3生成硝酸铁、NO和水;
B.硫酸氢钠与氢氧化钡按照物质的量之比为2:1反应生成硫酸钡、硫酸钠和水,溶液呈中性;
C.K37ClO3与浓盐酸在加热条件下生成氯气K37ClO3中37Cl全部被还原;
D.4mol偏铝根离子先与4盐酸反应生成4mol氢氧化铝,剩余3mol盐酸与1mol氢氧化铝反应生成氯化铝,所以得到产物为氢氧化铝沉淀和氯化铝混合物.
解答 解:A.Fe3O4溶于足量稀HNO3生成硝酸铁、NO和水,离子方程式:3Fe3O4+28H++NO3-=9Fe3++NO↑+14H2O,故A错误;
B.NaHSO4溶液与Ba(OH)2溶液混合至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故B错误;
C.K37ClO3与浓盐酸在加热条件下生成氯气K37ClO3中37Cl全部被还原生成氯气,所以不可能出现37Cl-,故C错误;
D.4mol•L-1的NaAlO2溶液与7mol•L-1的盐酸等体积互相均匀混合,离子方程式:4AlO2-+7H++H2O═3Al(OH)3↓+Al3+,故D正确;
故选:D.
点评 本题考查了离子方程式的正误判断,掌握离子方程式的书写原则,明确离子方程式正误判断常用方法是解题关键,注意反应物用量对反应的影响,选项D为易错选项,题目难度中等.

练习册系列答案
相关题目
16.下列指定反应的离子方程式正确的是( )
| A. | 向 H2O中通人 NO2:3NO2+H2O═H++NO3-+2NO | |
| B. | 向Na2SiO3溶液中通入少量SO2:Na2SiO3+SO2+H2O═H2SiO3↓+2Na++SO32- | |
| C. | 用饱和纯減溶液洗涤试管中残留的苯酚:CO32-+2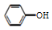 →2 →2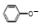 +CO2↑+H2O +CO2↑+H2O | |
| D. | 等体积等物质的量浓度的NH4Fe(SO4)2和Ba(OH)2混合:2Fe3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Fe(OH)3↓ |
13.下列有关卤族元素及其化合物的表示正确的是( )
| A. | 氟离子的结构示意图: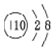 | |
| B. | 次氯酸分子的电子式: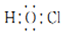 | |
| C. | 2,4,6-三溴苯酚的结构简式: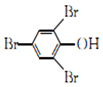 | |
| D. | 质子数为53,中子数为78的碘原子:5378I |
20.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1mol/L NaHSO4溶液中:K+、AlO2-、Cl-、CH3COO- | |
| B. | 0.1mol/L NaHCO3溶液中:Al3+、Ca2+、SO42-、NO3- | |
| C. | 0.1mol/L FeCl3溶液中:NH4+、NO3-、Na+、SO42 | |
| D. | 0.1mol/L H2O2溶液中:Na+、K+、SO42-、I- |
10.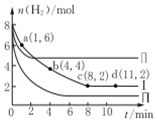 一定温度下向体积为2L的恒容密闭容器中充入6molCO2和8mo1H2,发生反应:CO2 (g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49KJ•mol-1.测得n(H2)物质的量随时间变化如曲线I 所示,下列说法正确的是( )
一定温度下向体积为2L的恒容密闭容器中充入6molCO2和8mo1H2,发生反应:CO2 (g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49KJ•mol-1.测得n(H2)物质的量随时间变化如曲线I 所示,下列说法正确的是( )
 一定温度下向体积为2L的恒容密闭容器中充入6molCO2和8mo1H2,发生反应:CO2 (g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49KJ•mol-1.测得n(H2)物质的量随时间变化如曲线I 所示,下列说法正确的是( )
一定温度下向体积为2L的恒容密闭容器中充入6molCO2和8mo1H2,发生反应:CO2 (g)+3H2(g)=CH3OH(g)+H2O(g)△H=-49KJ•mol-1.测得n(H2)物质的量随时间变化如曲线I 所示,下列说法正确的是( )| A. | 该反应在O~8min内的v(CO2)=0.125mol•L-1•min-1 | |
| B. | 若起始时向容器中充入3mo1CO2和4molH2,则平衡时CH3OH的体积分数大于20% | |
| C. | 若起始时向容器中充入4mo1CO2和2molH2、2molCH3OH、1molH2O(g),则此时反应v(正)>v(逆) | |
| D. | 曲线II、曲线III改变条件分别是升高温度、减小压强 |
17.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 在酒精灯上加热铝箔,铝箔熔化但不滴落 | 熔点:铝>氧化铝 |
| B | 向某溶液中先滴加KSCN溶液,再滴加少量氯水,先无明显现象,后溶液变成血红色 | 原溶液中含有Fe3+,没有Fe2- |
| C | KNO3和KOH混合溶液中加入铝粉并加热,管口放湿润的红色石蕊试纸,试纸变为蓝色 | NO3-还原为NH3 |
| D | 向加入了几滴酚酞试液的Na2CO3溶液中滴加BaCl2溶液,红色逐渐褪去 | Na2CO3溶液中存在水解平衡 |
| A. | A | B. | B | C. | C | D. | D |
5.下列分散系不能发生丁达尔效应的是( )
| A. | 氢氧化铁浊液 | B. | 豆浆 | C. | 含尘埃的空气 | D. | 墨水 |
6.某物质经分析只含有一种元素,则该物质不可能是( )
| A. | 单质 | B. | 化合物 | C. | 混合物 | D. | 纯净物 |