题目内容
20.对于放热反应H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,下列说法中,正确的是( )| A. | 生成物所具有的总能量高于反应物所具有的总能量 | |
| B. | 反应物所具有的总能量高于生成物所具有的总能量 | |
| C. | 断开1molH-H键和1molCl-Cl键所吸收的总能量大于形成2molH-Cl键所放出的能量 | |
| D. | 该反应中,化学能只转变为热能 |
分析 A.根据放热反应中反应物所具有的总能量高于产物所具有的总能量;
B.根据放热反应中反应物所具有的总能量高于产物所具有的总能量;
C.根据放热反应的本质是生成物成键释放的总能量大于反应物断键吸收的总能量;
D.根据放热反应中化学能转变为热能、光能等.
解答 解:A、反应是放热反应,则生成物所具有的总能量低于反应物所具有的总能量,故A错误;
B、反应放热,则反应物所具有的总能量高于生成物所具有的总能量,故B正确;
C、反应放热,则断开1 mol H-H键和1 mol Cl-Cl键所吸收的总能量小于形成2mol H-Cl键所放出的能量,故C错误;
D、反应还伴随发光,即没有完全都转化为热能,部分转化为光能,故D错误,
故选B.
点评 本题主要考查了化学反应的本质以及能量变化的宏观和微观原因,反应能量变化和物质能量高低的分析判断,题目难度不大.

练习册系列答案
相关题目
10.关于电化学的下列说法正确的是( )


| A. | 工业上用电解MgCl2溶液的方法冶炼Mg | |
| B. | 钢铁发生吸氧腐蚀的正极反应式为4OH--4e-═O2↑+2H2O | |
| C. | 如图中发生反应的方程式为:Fe+2H+=Fe2++H2↑ | |
| D. | 碱性锌锰干电池放电时的正极反应为:MnO2+H2O+e-=MnOOH+OH- |
11.下列各示意图与对应的表述不正确的是( )
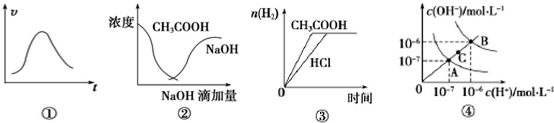

| A. | 图①可表示一定条件下,锌和稀硫酸反应的速率随时间变化的趋势图 | |
| B. | 图②中曲线表示将氢氧化钠溶液滴加到醋酸溶液中浓度的变化趋势图 | |
| C. | 图③表示等体积、等物质的量浓度的盐酸和醋酸,分别加足量镁粉,产生H2的物质的量变化 | |
| D. | 图④为水的电离平衡曲线图,若从A点到C点,可采用升高温度的方法 |
15.雾霾严重影响人们的生活与健康.某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.某同学收集了该地区的雾霾,经必要的预处理后试样溶液,设计并完成了如下的实验:
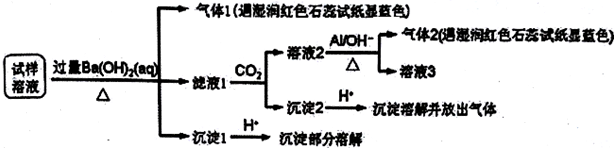
己知:3NO3-+8Al+5OH-+2H2O$\stackrel{△}{→}$3NH3+8AlO2-,根据以上的实验操作与现象,该同学得出的结论不正确的是( )

己知:3NO3-+8Al+5OH-+2H2O$\stackrel{△}{→}$3NH3+8AlO2-,根据以上的实验操作与现象,该同学得出的结论不正确的是( )
| A. | 试样中肯定存在NH4+、Mg2+、SO42-和NO3- | |
| B. | 该雾霾中可能存在NaNO3、NH4Cl和MgSO4 | |
| C. | 试样中可能存在Na+、Cl- | |
| D. | 试样中一定不含Al3+ |
9.用水稀释0.1 mol•L-1 CH3COOH时,溶液中随着水量的增加而减小的是( )
| A. | $\frac{c(C{H}_{3}COOH)}{c(O{H}^{-})}$ | B. | $\frac{c(O{H}^{-})}{c({H}^{+})}$ | C. | c(H+)和c(OH-)的乘积 | D. | OH-的物质的量 |
10.下列离子方程式正确的是( )
| A. | 纯碱溶液显碱性:CO32-+2H2O?H2CO3+2OH- | |
| B. | 醋酸溶液显酸性:CH3COOH+H2O?CH3COO-+H3O+ | |
| C. | 向碘化亚铁溶液中通入足量的溴水:2 Br2+2Fe2++2I-═4Br-+2Fe3++I2 | |
| D. | 向碳酸氢钙溶液中滴加过量的烧碱溶液:HCO3-+Ca2++2OH-═CaCO3↓+H2O |