题目内容
2.研究CO2的利用对促进低碳社会的构建具有重要意义.(1)将CO2与焦炭作用生成CO,CO可用于炼铁等.
已知:①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ•mol-1
则CO还原Fe2O3(s)的热化学方程式为Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1.
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H
①该反应的平衡常数表达式为K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$.
②取一定体积CO2和H2的混合气体(物质的量之比为1:3),加入恒容密闭容器中发生上述反应,反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的△H<0(填“>”、“<”或“=”).
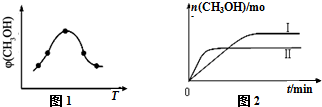
③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线Ⅰ、Ⅱ对应的平衡常数大小关系为KⅠ>KⅡ(填“>”、“<”或“=”).
(3)以CO2为原料还可以合成多种物质.
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其发生可逆反应的方程式为2NH3+CO2$\frac{\underline{\;一定条件\;}}{\;}$CO(NH2)2+H2O.
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,请写出该电极反应的方程式为CO2+8e-+8H+=CH4+2H2O.
分析 (1)依据热化学方程式和盖斯定律计算得到所需热化学方程式,①-②×3得到Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)和反应焓变;
(2)①依据化学方程式和平衡常数概念写出平衡常数表达式,平衡常数=$\frac{生成物平衡浓度系数次幂之积}{反应物平衡浓度系数次幂之积}$;
②由图可知最高点反应到达平衡,到达平衡后,温度越高,φ(CH3OH)越小,升高温度平衡向逆反应进行,据此判断;
③由图象分析先拐先平,温度高TⅡ先达到平衡则TⅡ>TⅠ,纵轴是甲醇的物质的量,温度越高,甲醇越少,平衡逆向进行分析判断;
(3)①根据反应物、反应条件、生成物写出,反应物是二氧化碳和氨气(NH3),反应条件是高温、高压,生成物是尿素[CO(NH2)2]和水;
②根据原电池原理,CO2在正极发生还原反应转化为甲烷,注意电解质溶液为酸性.
解答 解:(1)①Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H1=+489.0kJ•mol-1
②C(石墨)+CO2(g)=2CO(g)△H2=+172.5kJ•mol-1
依据盖斯定律①-②×3得到Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1;
故答案为:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)△H=-28.5 kJ•mol-1;
(2)①平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以K=$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$,
故答案为:$\frac{c(C{H}_{3}OH)•c({H}_{2}O)}{c(C{O}_{2})•{c}^{3}({H}_{2})}$;
②由图可知最高点反应到达平衡,达平衡后,温度越高,φ(CH3OH)越小,平衡向逆反应进行,升高温度平衡吸热方向进行,逆反应为吸热反应,则正反应为放热反应,即△H<0,
故答案为:<;
③由图2可知,温度TⅠ<TⅡ,平衡时,温度越高CO的转化率越小,说明升高温度,平衡向逆反应移动,升高温度平衡向吸热反应移动,故该反应正反应为放热反应,则△H<0,升高温度,平衡向逆反应移动,所以KⅠ>KⅡ,
故答案为:>;
(3)①根据反应物是二氧化碳和氨气(NH3),反应条件是高温、高压,生成物是尿素[CO(NH2)2]和水,化学反应式为2NH3+CO2$\frac{\underline{\;一定条件\;}}{\;}$CO(NH2)2+H2O,
故答案为:2NH3+CO2$\frac{\underline{\;一定条件\;}}{\;}$CO(NH2)2+H2O;
②CO2在正极发生还原反应转化为甲烷,考虑电解质为硫酸,所以甲烷中氢来源为硫酸电离的氢离子,根据化合价变化可知1mol二氧化碳变成甲烷得到8mol电子,故电极反应为:CO2+8e-+8H+=CH4+2H2O,
故答案为:CO2+8e-+8H+=CH4+2H2O.
点评 本题考查了热化学方程式的书写、化学平衡移动、平衡常数概念理解、转化率的计算及原电池原理的分析应用等,题目涉及的知识点较多,综合性较强,难度中等.分析图象时,要考虑先拐先平衡的原则,则反应条件为温度高或压强大,写电极反应式一定要考虑介质的参与.

②NaH+H2O=NaOH+H2↑
③2Na+2H2O=2NaOH+H2↑,
④2F2+2H2O=4HF+O2
有关上述反应叙述不正确的是( )
| A. | 离子半径:N3->F->Na+ | |
| B. | 上述反应除①外都是氧化还原反应 | |
| C. | 反应②③中的水做氧化剂,每生成1mol H2,转移的电子数为2NA | |
| D. | 反④中的水是还原剂 |
| A. | 在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解 | |
| B. | Fe(OH)3胶体无色、透明,能发生丁达尔现象 | |
| C. | H2、SO2、CO2三种气体都可用浓硫酸干燥 | |
| D. | Na2O和Na2O2投入水中都能生成NaOH,都是氧化还原反应,它们都是碱性氧化物 |
| A. | 体积之比是2:3 | B. | 原子数之比是3:2 | ||
| C. | 质子数之别是1:1 | D. | 物质的量之比是1:1 |
| A. | 标准状况下,22.4L水所含有的原子数目为3NA | |
| B. | 标准状况下,22.4 L H2中含质子数为2NA | |
| C. | 0.1mol•L-1稀硫酸100mL中含有硫酸根个数为0.1NA | |
| D. | 0.1molOH-含NA个电子 |
| 实验编号 | ① | ② | ③ | ④ |
| 稀硝酸体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属质量/g | 9.0 | 4.8 | 0 | 0 |
| NO体积/L | 1.12 | 2.24 | 3.36 | V |
(1)硝酸的浓度为多少?
(2)③中溶解的Cu的质量为多少?
(3)④中的V为多少?
①4HCl(浓)+MnO2 $\frac{\underline{\;\;△\;\;}}{\;}$ nCl2+Cl2↑+2H2O
②4HCl(g)+O2 $\frac{\underline{\;催化剂\;}}{△}$2Cl2+2H2O(g)
③2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O
则三种氧化剂氧化性由强到弱的顺序是( )
| A. | O2 MnO2 KMnO4 | B. | KMnO4 MnO2O2 | ||
| C. | MnO2KMnO4 O2 | D. | O2 KMnO4 MnO2 |
| A. | 酒精和水 | B. | 汽油和水 | C. | 苯和水 | D. | 四氯化碳和水 |
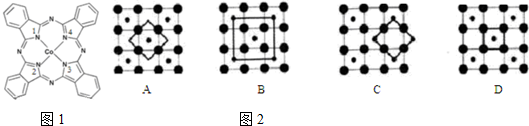
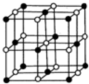 ),在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如2所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是D.
),在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在 5K 下呈现超导性的晶体,该晶体具有CoO2的层状结构(如2所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述CoO2的化学组成的是D.