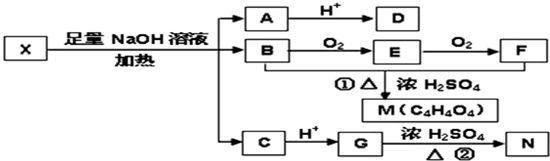
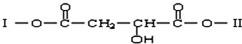题目内容
若NA表示阿伏伽德罗常数,则下列说法正确的是( )
| A、1molFe在氧气中完全燃烧后,失去了3NA个电子 |
| B、1mol白磷含3NA个P-P键 |
| C、1mol二氧化硅中含2NA个Si-O键 |
| D、石墨晶体每层内任意一个碳原子都与其他三个碳原子以共价键结合,形成平面网状结构 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.铁在氧气中燃烧生成四氧化三铁;
B.根据P4是正四面体结构进行分析;
C.根据1mol二氧化硅中含有4mol硅氧键进行计算;
D.依据石墨晶体结构解答.
B.根据P4是正四面体结构进行分析;
C.根据1mol二氧化硅中含有4mol硅氧键进行计算;
D.依据石墨晶体结构解答.
解答:
解:A.1mol铁在氧气中燃烧生成四氧化三铁,四氧化三铁中铁元素的平均化合价为
价,则失去的电子为
mol,故A错误;
B.P4是正四面体结构,1mol P4含有P-P键含有6mol共价键,含有p-P键的个数为6NA,故B错误;
C.1mol二氧化硅中含有1mol硅原子,形成了4mol硅氧键,含有的Si-O键数目为4NA,故C错误;
D.石墨晶体为层状结构,层与层之间通过分子间作用力结合,每层内任意一个碳原子都与其他三个碳原子以共价键结合成平面正六边形结构,故D正确;
故选:D.
| 8 |
| 3 |
| 8 |
| 3 |
B.P4是正四面体结构,1mol P4含有P-P键含有6mol共价键,含有p-P键的个数为6NA,故B错误;
C.1mol二氧化硅中含有1mol硅原子,形成了4mol硅氧键,含有的Si-O键数目为4NA,故C错误;
D.石墨晶体为层状结构,层与层之间通过分子间作用力结合,每层内任意一个碳原子都与其他三个碳原子以共价键结合成平面正六边形结构,故D正确;
故选:D.
点评:本题考查了阿伏伽德罗常数,侧重对物质空间结构的考查,熟悉白磷、二氧化硅、石墨结构是解题关键,题目难度中等.

练习册系列答案
相关题目
化学与生活密切相关.下列情况会对人体健康造成较大危害的是( )
| A、用Cl2对自来水进行消毒杀菌 |
| B、用SO2漂白食品 |
| C、用食醋清洗热水瓶胆内壁附着的水垢(CaCO3) |
| D、用小苏打(NaHCO3)发酵面团制作馒头 |
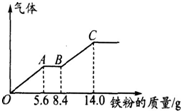 某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )
某稀硫酸和稀硝酸的混合溶液200mL,平均分成两份.向其中一份中逐渐加入铜粉,最多能溶解9.6g.向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体).下列分析或结果错误的是( )| A、H2SO4浓度为2.5 mol?L-1 |
| B、第二份溶液中最终溶质为FeSO4 |
| C、OA段产生的是NO,AB段的反应为Fe+2Fe3+═3Fe2+,BC段产生氢气 |
| D、原混合酸中NO3-物质的量为0.1mol |
分析发现,某陨石中含有半衰期极短的镁的一种放射性同位素28Mg,该同位素的原子核内的中子数是( )
| A、12 | B、14 | C、16 | D、18 |
只给出表中甲和乙对应的量,不能用来求物质的量的是( )
| 甲 | 乙 | |
| A | 物质的微粒数 | 阿伏加德罗常数 |
| B | 标准状况下气体摩尔体积 | 标准状况下气体体积 |
| C | 固体体积 | 固体密度 |
| D | 非标准状况下物质的质量 | 物质的摩尔质量 |
| A、A | B、B | C、C | D、D |
下列有关化学用语使用正确的是( )
A、HClO的电子式:H:
| ||||||||
B、具有16个质子、16个中子和18个电子的微粒是
| ||||||||
C、邻羟基苯甲酸的结构简式: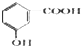 | ||||||||
D、乙烯的比例模型: |
分类是学习和研究化学的一种常用的科学方法.下列分类合理的是( )
| A、根据酸分子中含氢原子个数将酸分为一元酸、二元酸等 |
| B、根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 |
| C、根据元素原子最外层电子数的多少将元素分为金属和非金属 |
| D、根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质 |