题目内容
20.我国材料科学家师昌绪在合金钢、高温合金及材料强度的研究领域作出了杰出贡献,荣获2010年度国家最高科学技术奖.①合金是生活中常见的材料.某合金具有密度小、强度高的优良性能,常用于制造门窗框架.该合金中含量最高的金属元素的原子结构示意图为
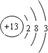 .
.②铁锈的主要成分是Fe2O3•xH2O(填化学式),它是钢铁在潮湿的空气中发生电化学腐蚀的结果.
③玻璃是一种常用的硅酸盐材料.制备普通玻璃的原料有Na2CO3、CaCO3和SiO2(填化学式).
分析 ①根据该金属常用于制造门窗框架.可知为铝,然后写出原子结构示意图;
②钢铁在潮湿的空气中发生吸氧腐蚀;
③工业制玻璃主要原料有石英、纯碱和石灰石.
解答 解:①铝原子结构示意图为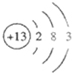 ,故答案为:
,故答案为: ;
;
②铁锈的成分为Fe2O3•xH2O,钢铁在潮湿的空气中发生吸氧腐蚀,属于电化学腐蚀,故答案为:Fe2O3•xH2O;电化学;
③工业制玻璃主要原料有石英、纯碱和石灰石,故答案为:CaCO3;SiO2.
点评 本题考查化学与环境、材料、信息、能源关系密切相关的知识,为高频考点,侧重于基础知识的综合理解和运用的考查,难度不大.

练习册系列答案
相关题目
11.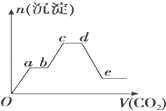 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是( )
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是( )
 将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是( )
将足量的CO2不断通入KOH、Ba(OH)2、KAlO2的混合溶液中,生成沉淀的物质的量与所通入CO2的体积关系如图所示.下列关于整个反应过程中的叙述不正确的是( )| A. | Oa段反应的化学方程式是Ba(OH)2+CO2═BaCO3↓+H2O | |
| B. | ab段与cd段沉淀质量都不变,但所发生的反应不相同 | |
| C. | bc段反应的离子方程式是:2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- | |
| D. | de段沉淀减少是由于Al(OH)3固体消失的 |
9.已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,下列说法正确的是( )
| A. | 2 L氨气体分解成1 L氮气与3 L氢气吸收92 kJ热量 | |
| B. | 1 mol氮气与3 mol氢气反应生成2 mol液态氨放出的热量小于92 kJ | |
| C. | 25℃和101kPa时,2 molNH3(g)完全分解为1 mol N2(g)和3 mol H2(g )吸热92KJ | |
| D. | 3个氢气分子与1个氮气分子反应生成2个氨气分子放出92 kJ热量 |

 .
. .
.