题目内容
低碳经济是以低能耗、低污染、低排放为基础的经济模式,是人类社会继农业文明、工业文明之后的又一次重大进步.低碳经济实质是能源高效利用、清洁能源开发、追求绿色GDP的问题,核心是能源技术和减排技术创新.科学家预测“氢能”作为一种清洁能源,将是未来最理想的新能源.请回答下列问题:
(1)实验测得,1克氢气燃烧生成液态水放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为 .
A.2H2(g)+O2(g)=2H2O(l);△H=-142.9kJ/mol
B.H2(g)+
O2(g)=H2O(l);△H=-285.8kJ/mol
C.2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol
D.H2(g)+
O2(g)=H2O(g);△H=-285.8kJ/mol
(2)根据“绿色化学”的思想,为了制备H2,某化学家设计了下列化学反应步骤:
①CaBr2+H2O
CaO+2HBr ②2HBr+Hg
HgBr2+H2↑
③HgBr2+CaO
HgO+CaBr2 ④2HgO
2Hg+O2↑
上述过程的总反应可表示为 .
(3)电解水制取H2需要消耗大量的电能,接收太阳能分解水得到氢气是人类开发氢能源的主要研究课题.已知在特定条件下聚合太阳能所得高温可使氢碘酸分解出氢气,也可使硫酸分解出氧气.下图是国外正在研究中的一种利用核能把水分解,制取氢气的一种流程(硫-碘热循环法).
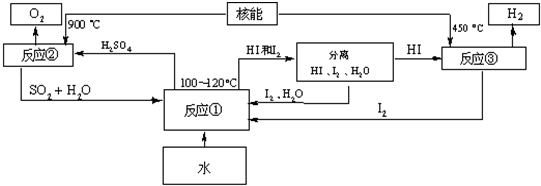
请写出反应①的化学方程式: .
用硫-碘热循环法制取氢气,非常符合低碳经济理念,其原因是①采用新能源技术且能量利用率高② .
(4)已知用电解法生产1立方米的氢气(标准状况)大约消耗400度电,则用上述硫-碘热循环法产生103kg氢气,相当于减排CO2 吨(二氧化碳排放量(kg)=耗电度数×0.785).
(1)实验测得,1克氢气燃烧生成液态水放出142.9kJ热量,则表示氢气燃烧热的热化学方程式为
A.2H2(g)+O2(g)=2H2O(l);△H=-142.9kJ/mol
B.H2(g)+
| 1 |
| 2 |
C.2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ/mol
D.H2(g)+
| 1 |
| 2 |
(2)根据“绿色化学”的思想,为了制备H2,某化学家设计了下列化学反应步骤:
①CaBr2+H2O
| ||
| ||
③HgBr2+CaO
| ||
| ||
上述过程的总反应可表示为
(3)电解水制取H2需要消耗大量的电能,接收太阳能分解水得到氢气是人类开发氢能源的主要研究课题.已知在特定条件下聚合太阳能所得高温可使氢碘酸分解出氢气,也可使硫酸分解出氧气.下图是国外正在研究中的一种利用核能把水分解,制取氢气的一种流程(硫-碘热循环法).

请写出反应①的化学方程式:
用硫-碘热循环法制取氢气,非常符合低碳经济理念,其原因是①采用新能源技术且能量利用率高②
(4)已知用电解法生产1立方米的氢气(标准状况)大约消耗400度电,则用上述硫-碘热循环法产生103kg氢气,相当于减排CO2
考点:用盖斯定律进行有关反应热的计算,化学方程式的书写
专题:
分析:(1)燃烧热的热化学方程式中可燃物物质的量为1moL,生成稳定的氧化物,水的状态为液态;
(2)总反应可由分步反应相加减得到;
(3)由图知:反应物为:SO2,I2,H2O,生成物为:HI,H2SO4;
(4)设产生103kg氢气,相当于减排CO2 X吨,结合题中信息列方程求解.
(2)总反应可由分步反应相加减得到;
(3)由图知:反应物为:SO2,I2,H2O,生成物为:HI,H2SO4;
(4)设产生103kg氢气,相当于减排CO2 X吨,结合题中信息列方程求解.
解答:
解:(1)1克氢气燃烧生成液态水放出142.9kJ热量,1moL放出的热量为285.8kJ,燃烧热的热化学方程式中可燃物物质的量为1moL,生成稳定的氧化物,水的状态为液态,故选B.
(2)①CaBr2+H2O
CaO+2HBr ②2HBr+Hg
HgBr2+H2↑
③HgBr2+CaO
HgO+CaBr2 ④2HgO
2Hg+O2↑
将(①+②+③)×2+④,得:2H2O
2H2↑+O2↑,
故答案为:2H2O
2H2↑+O2↑;
(3)由图知:反应物为:SO2,I2,H2O,生成物为:HI,H2SO4,故方程式为:SO2+I2+2H2O
2HI+H2SO4,
H2SO4可分解为SO2,O2,H2O,SO2和I2可循环使用,故答案为:SO2+I2+2H2O
2HI+H2SO4,SO2和I2可循环使用,无污染;
(4)设产生103kg氢气,相当于减排CO2 X吨,则
×22.4×10-3×400×0.785=X×103,解得X=3516.8,故答案为3516.8;
(2)①CaBr2+H2O
| ||
| ||
③HgBr2+CaO
| ||
| ||
将(①+②+③)×2+④,得:2H2O
| ||
| △ |
故答案为:2H2O
| ||
| △ |
(3)由图知:反应物为:SO2,I2,H2O,生成物为:HI,H2SO4,故方程式为:SO2+I2+2H2O
| ||
H2SO4可分解为SO2,O2,H2O,SO2和I2可循环使用,故答案为:SO2+I2+2H2O
| ||
(4)设产生103kg氢气,相当于减排CO2 X吨,则
| 10 3×103 |
| 2 |
点评:本题考查热化学方程式的判断与方程式的书写,新能源的使用,难度不大.

练习册系列答案
相关题目
在3NO2+H2O═2HNO3+NO中,还原剂与氧化剂的物质的量之比为( )
| A、3:1 | B、1:3 |
| C、2:1 | D、1:2 |
最新研究表明:NO吸收治疗法可快速改善SARS重症患者的缺氧状况,缓解病情.病毒学研究同时证实,NO对SARS病毒有直接抑制作用.下列叙述正确的是( )
| A、NO是一种红棕色的气体 |
| B、常温常压下,NO不能与空气中氧气直接化合 |
| C、含等质量的氧元素的NO和CO的物质的量相等 |
| D、NO易溶于水,不能用排水法收集 |
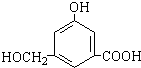 如图有机物具有多种官能团,因而能跟多种物质反应,但因其分子内的羧基与醇羟基、酚羟基间“位阻”较大,故不能发生分子内的酯化反应,试写出该有机物发生下列反应的方程式:
如图有机物具有多种官能团,因而能跟多种物质反应,但因其分子内的羧基与醇羟基、酚羟基间“位阻”较大,故不能发生分子内的酯化反应,试写出该有机物发生下列反应的方程式: