题目内容
17.对于金属冶炼的工业方法,下列有关说法中正确的是( )| A. | 可用电解饱和的MgCl2溶液的方法获得金属镁 | |
| B. | 电解CuSO4溶液精炼金属铜时,用铁做阳极 | |
| C. | 电解熔融Al2O3方法冶炼金属铝时,同时要加入冰晶石作助熔剂 | |
| D. | 工业上常采用活泼金属还原法冶炼金属银 |
分析 A.电解饱和氯化镁溶液,阳极上氢氧根离子放电生成氧气,阴极氢离子得到电子生成氢气,反应生成氢氧化镁;
B.电解精炼铜需要粗铜做阳极,精铜做阴极;
C.工业上电解熔融氧化铝在阴极析出金属铝,阳极上得到氧气,加入冰晶石是降低氧化铝熔点;
D.金属的活动性不同,可以采用不同的冶炼方法.
金属冶炼的方法主要有:
热分解法:对于不活泼金属,可以直接用加热分解的方法将金属从其化合物中还原出来(Hg及后边金属);
热还原法:在金属活动性顺序表中处于中间位置的金属,通常是用还原剂(C、CO、H2、活泼金属等)将金属从其化合物中还原出来(Zn~Cu);
电解法:活泼金属较难用还原剂还原,通常采用电解熔融的金属化合物的方法冶炼活泼金属(K~Al).
解答 解:A.Mg是活泼金属,应该采用电解熔融氯化镁的方法冶炼,如果电解氯化镁溶液,阴极上氢离子放电而不是镁离子放电,所以得不到Mg,故A错误;
B.如果Fe作阳极,电解硫酸铜溶液时,阳极上Fe失电子发生氧化反应,阴极上铜离子得电子发生还原反应,应粗铜做阳极,精铜做阴极进行精炼,故B错误;
C.电解熔融Al2O3方法冶炼金属铝时,氧化铝熔点较高,加入冰晶石作熔剂时能降低熔融温度,从而减少能源浪费,故C正确;
D.Ag属于不活泼金属,应该采用热分解法冶炼,故D错误;
故选C.
点评 本题考查金属的冶炼,明确金属活泼性强弱与冶炼方法选取的关系是解本题关键,题目难度不大,注意电解氯化镁溶液不能得到金属镁.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
8.下列反应中生成物总能量高于反应物总能量的是( )
| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | ||
| C. | 盐酸与氢氧化钠中和 | D. | 氧化钙溶于水 |
5.下列选项中属于同位素关系的是( )属于同素异形体关系的是( )
| A. | O2,O3,O4 | B. | 40Ca,40Ar | C. | Fe2+,Fe3+ | D. | 氕,氘,氚 | ||||
| E. | H2O,D2O,T2O | F. | H2,D2,T2 | G. | Na,Na+ |
2.下列电离方程式不正确的是( )
| A. | NH4NO3=NH4++NO3- | B. | CH3COOH=H++CH3COO- | ||
| C. | NH3•H2O?NH4++OH- | D. | NaHCO3=Na++HCO3- |
9.元素及其化合物丰富了物质世界,下列说法不正确的是( )
| A. | 除去FeCl2溶液中的FeCl3,可向溶液中加入足量铁粉,反应后过滤 | |
| B. | NaOH溶液和AlCl3溶液相互滴加的现象不同 | |
| C. | 用热的纯碱溶液洗碗可去除油污 | |
| D. | 将浓硫酸滴到白纸上,白纸变黑了,说明浓硫酸具有吸水性 |
6.下列实验装置进行相应的实验,不能达到实验目的是( )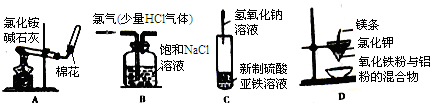

| A. | 实验室制取并收集氨气 | B. | 除去Cl2中的HCl气体杂质 | ||
| C. | 实验室制取氢氧化亚铁 | D. | 铝热反应实验 |
7.中学化学常见物质存在转化关系:A+B→C+D+H2O,其中C属于盐类,下列推断不正确的是( )
| A. | 若A为黄绿色气体,则D可能有漂白性 | |
| B. | 若A为红色金属单质,则D一定是红棕色气体 | |
| C. | 若A为纯碱,则D一定能使澄清石灰水变浑浊 | |
| D. | 若A为氯化铵,则D一定是具有刺激性气味的气体 |