题目内容
热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是( )
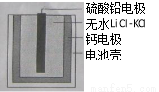
A.正极反应式:Ca+2Cl- - 2e- = CaCl2
B.常温时,在正负极间接上电流表或检流计,指针不偏转
C.放电过程中,Li+向负极移动
D.每转移0.1mol电子,理论上生成20.7g Pb
B
【解析】
试题分析:A、正极发生还原反应,根据总反应方程式可知,发生还原反应的是PbSO4,所以正极反应式为PbSO4+2e- =Pb+SO42-,错误;B、该电池中的电解质在受热熔融后,即可瞬间输出电能,而常温下电解质是固态,没有自由移动的离子,不能产生电流,所以指针不偏转,正确;C、放电时,阳离子向正极移动,错误;D、每转移0.1mol电子,理论上生成0.05molPb,质量是10.35g,错误,答案选B。
考点:考查原电池的反应原理,电极反应式的判断,氧化还原反应的计算

练习册系列答案
相关题目
化学与社会、生活密切相关。对下列现象或事实的解释正确的是( )
选项 | 现象或事实 | 解 释 |
A | 用浸泡酸性高锰酸钾溶液的硅土延长果实的成熟 | 利用乙烯可以发生加成反应
|
B | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低肥效 |
C | SO2能使品红溶液褪色 | SO2具有还原性 |
D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |