题目内容
下列叙述中,正确的是( )
| A、硫酸的摩尔质量是98g |
| B、1mol N2的质量是28g/mol |
| C、阿伏加德罗常数是6.02×1023 |
| D、标准状况下,气体的摩尔体积约为22.4L/mol |
考点:摩尔质量,阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、摩尔质量的单位是g/mol;
B、质量的单位是g;
C、阿伏伽德罗常数的单位为mol-1;
D、标准状况下,气体的摩尔体积约为22.4L/mol.
B、质量的单位是g;
C、阿伏伽德罗常数的单位为mol-1;
D、标准状况下,气体的摩尔体积约为22.4L/mol.
解答:
解:A、摩尔质量的单位是g/mol,硫酸的摩尔质量是98g/mol,故A错误;
B、质量的单位是g,1mol N2的质量是28g,故B错误;
C、阿伏伽德罗常数的单位为mol-1,阿伏加德罗常数是6.02×1023mol-1,故C错误;
D、标准状况下,气体的摩尔体积约为22.4L/mol,故D正确.
故选:D.
B、质量的单位是g,1mol N2的质量是28g,故B错误;
C、阿伏伽德罗常数的单位为mol-1,阿伏加德罗常数是6.02×1023mol-1,故C错误;
D、标准状况下,气体的摩尔体积约为22.4L/mol,故D正确.
故选:D.
点评:本题考查了摩尔质量和气体摩尔体积、阿伏伽德罗常数的概念及应用,难度不大,注意基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将铁片和锌片放在盛有NaCl溶液(其中滴有酚酞)的表面皿中,如图所示,最先观察到变为红色的区域为( )
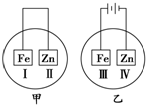

| A、Ⅰ和Ⅱ | B、Ⅰ和Ⅳ |
| C、Ⅱ和Ⅲ | D、Ⅱ和Ⅳ |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol NaHSO4晶体中离子总数为3NA |
| B、2.24 L 14CH4分子中所含中子数为0.8NA |
| C、0.1 L 3 mol?L-1的NH4NO3溶液中含有的NH4+数目为0.3NA |
| D、标准状况下,将FeSO4溶液置于空气中,被氧化的Fe2+为0.2NA,吸收O2为1.12 L |
下列反应能用离子方程式CO32-+2H+=CO2↑+H2O表示的是( )
| A、NaHCO3+HCl=NaCl+CO2↑+H2O |
| B、BaCO3+2HCl=BaCl2+H2O+CO2↑ |
| C、Na2CO3+H2SO4=Na2SO4+CO2↑+H2O |
| D、K2CO3+2CH3COOH=2CH3COOK+CO2↑+H2O |
日常生活中遇到的很多问题都涉及到化学知识,下列有关叙述不正确的是( )
| A、用纯碱溶液洗涤餐具上的油污 |
| B、用食盐水清洗热水瓶中的水垢 |
| C、食盐中添加适量KIO3 |
| D、利用丁达尔效应区别蛋白质溶液和食盐溶液 |
根据下列反应判断还原剂的还原性由强到弱的顺序,正确的是( )
①Cl2+2KI═I2+2KCl
②2FeCl3+2HI═I2+2FeCl2+2HCl
③2FeCl2+Cl2═2FeCl3
④I2+SO2+2H2O═2HI+H2SO4.
①Cl2+2KI═I2+2KCl
②2FeCl3+2HI═I2+2FeCl2+2HCl
③2FeCl2+Cl2═2FeCl3
④I2+SO2+2H2O═2HI+H2SO4.
| A、SO2>I->Fe2+>Cl- |
| B、Cl2>Fe3+>I2>SO2 |
| C、Fe2+>Cl->I->SO2 |
| D、Cl->Fe2+>I->SO2 |
设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A、标准状况下,22.4LH2O所含有的原子数目为3NA |
| B、标准状况下,22.4 L H2中含质子数为2NA |
| C、100mL 0.1mol?L-1稀硫酸中含有硫酸根个数为0.1NA |
| D、常温常压下,48 g 03含有的氧原子数为NA |
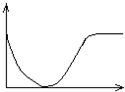 下列实验过程中产生的现象与右边坐标图形相符合的是( )
下列实验过程中产生的现象与右边坐标图形相符合的是( )