题目内容
18.有A、B、C、D四瓶溶液,它们是硫酸钠,亚硫酸钠、盐酸和氯化钡溶液.为了鉴别它们,各取少量溶液进行两两反应,结果如表所示,表中“↓”表示有沉淀或微溶物质生成,“↑”表示有气体生成,“-”表示无明显现象.由此可以推断它们的组成为:AHCl;BBaCl2;CNa2SO4;DNa2SO3.| A | B | C | D | |
| A | - | - | ↑ | |
| B | - | ↓ | ↓ | |
| C | - | ↓ | - | |
| D | ↑ | ↓ | - |
分析 A、B、C、D四瓶溶液,分别是Na2SO4、Na2SO3、HCl、BaCl2,A与其它物质反应只有一个有气体产生,其它都没有现象,所以A为HCl,D为Na2SO3,产生的气体为二氧化硫,B与其它物质反应有两个沉淀的现象,所以B为BaCl2,分别产生硫酸钡沉淀和亚硫酸钡沉淀,C与其它物质反应只有一个有沉淀现象,所以C为Na2SO4,亚硫酸钠与盐酸有气体,与氯化钡有沉淀,符合题中各物质间反应的现象,据此答题;
解答 解:A、B、C、D四瓶溶液,分别是Na2SO4、Na2SO3、HCl、BaCl2,A与其它物质反应只有一个有气体产生,其它都没有现象,所以A为HCl,D为Na2SO3,产生的气体为二氧化硫,B与其它物质反应有两个沉淀的现象,所以B为BaCl2,分别产生硫酸钡沉淀和亚硫酸钡沉淀,C与其它物质反应只有一个有沉淀现象,所以C为Na2SO4,亚硫酸钠与盐酸有气体,与氯化钡有沉淀,符合题中各物质间反应的现象,综上所述,A为HCl,B为BaCl2,C为Na2SO4,D为Na2SO3,
故答案为:HCl;BaCl2;Na2SO4;Na2SO3.
点评 本题考查无机物的推断,为高频考点,把握物质的性质、物质之间的反应及现象为解答的关键,侧重分析与推断能力的考查,注意A、B物质为推断的突破口,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.下列对化学用语的理解正确的是( )
| A. | 结构示意图 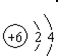 :表示碳原子 :表示碳原子 | |
| B. | 比例模型 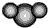 :表示二氧化碳分子 :表示二氧化碳分子 | |
| C. | 电子式 :表示羟基 :表示羟基 | |
| D. | H++OH-═H2O:表示醋酸和氢氧化钠的反应 |
9.下列说法正确的是( )
| A. | 增大反应物浓度可以增大活化分子百分数,从而使反应速率增大 | |
| B. | 汽车尾气的催化转化装置可将尾气中的NO和CO等有害气体快速地转化为N2和CO2,其原因是催化剂可增大NO和CO反应的活化能 | |
| C. | 在“反应热的测量实验”中测定反应后温度的操作方法:将量筒中的NaOH溶液经玻璃棒引流缓缓倒入盛有盐酸的简易量热计中,立即盖上盖板,并用环形玻璃搅拌棒不断搅拌,准确读出并记录反应体系的最高温度 | |
| D. | 研制性能优良的催化剂既可以提高化学反应速率,又能起到很好的节能效果 |
13.下列各组离子在水溶液中不是因为水解而不能大量共存的是( )
| A. | K+、Ca2+、HCO3-、Br- | B. | SO32-、Al(OH)4-、K+、Al3+ | ||
| C. | Fe3+、Na+、NO3-、CO32- | D. | NH4+、Na+、SiO32-、I- | ||
| E. | Ca2+、Na+、NO3-、PO43- |
3.下列说法正确的( )
| A. | 将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol•L-1 | |
| B. | 18gH2O在标准状况下的体积是22.4L | |
| C. | 22.4LO2中一定含有6.02×1023个氧分子 | |
| D. | 在标准状况时,20mLNH3与60mLNO所含的原子个数比为2:3 |
10.某学生做完实验后,采用下列方法清洗所用仪器:
①用稀硝酸清洗做过银镜反应后的试管
②用酒精清洗做过碘升华的烧杯
③用浓盐酸清洗做过高锰酸钾分解实验的试管
④用盐酸清洗长期存放三氯化铁溶液的试剂瓶
⑤用氢氧化钠溶液清洗沾有硫磺的试管
下列对以上操作的判断.正确的是( )
①用稀硝酸清洗做过银镜反应后的试管
②用酒精清洗做过碘升华的烧杯
③用浓盐酸清洗做过高锰酸钾分解实验的试管
④用盐酸清洗长期存放三氯化铁溶液的试剂瓶
⑤用氢氧化钠溶液清洗沾有硫磺的试管
下列对以上操作的判断.正确的是( )
| A. | 除④外都对 | B. | 除⑤外都对 | C. | ④⑤不对 | D. | 全都正确 |