题目内容
 氢气是一种新型的绿色能源,又是一种重要的化工原料.
氢气是一种新型的绿色能源,又是一种重要的化工原料.合成氨反应的热化方程式如下:
N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol
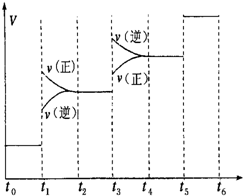
(1)当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如图所示.
图中t1时引起平衡移动的条件可能是
其中表示平衡混合物中NH3的含量最高的一段时间是
(2)若在恒温、恒压条件下向平衡体系中通入氩气,平衡
(3)温度为T℃时,将2a mol H2和 a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则反应的平衡常数为
考点:化学反应速率变化曲线及其应用,化学平衡的影响因素
专题:化学平衡专题
分析:(1)根据图象分析影响平衡的因素,平衡常数随温度而变化;
(2)依据影响平衡的因素分析判断平衡移动;
(3)计算出平衡时各物质的浓度,根据平衡常数表达式计算化学平衡常数等于生成物浓度幂之积与反应物浓度幂之积的比
(2)依据影响平衡的因素分析判断平衡移动;
(3)计算出平衡时各物质的浓度,根据平衡常数表达式计算化学平衡常数等于生成物浓度幂之积与反应物浓度幂之积的比
解答:
(1)N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol;反应是放热反应,反应前后气体体积减小,依据反应速率与时间的关系图象分析,t1时正逆反应速率都增大,平衡正向移动,引起平衡移动的条件可能是增大压强;表示平衡混合物中NH3的含量最高的一段时间是t2-t3;若t0-t1,t1-t3,t3-t5这三段平衡常数分别用K1,K2,K3表示,平衡常数随温度变化,升高温度平衡左移,平衡常数减小,那么K1,K2,K3的大小关系是:K1=K2>K3,
故答案为:增大压强;t2-t3;K1=K2>K3;
(2)若在恒温、恒压条件下向平衡体系中通入氩气,为保持恒压,体积增大,平衡向逆向进行;催化剂改变反应速率,不改变化学平衡,反应焓变不变,故答案为:向左;不改变;
(3)温度为T℃时,将2a mol H2和 a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则反应的平衡常数可以列出三段式计算平衡浓度,依据平衡常数概念计算:
N2(g)+3H2(g)?2NH2(g)
开始 2amol/L 4amol/L 0
反应 amol/L 3amol/L 2amol/L
平衡 amol/L amol/L 2amol/L
所以化学平衡常数K=
=
(mol/L)-2;
故答案为:
(mol/L)-2;
故答案为:增大压强;t2-t3;K1=K2>K3;
(2)若在恒温、恒压条件下向平衡体系中通入氩气,为保持恒压,体积增大,平衡向逆向进行;催化剂改变反应速率,不改变化学平衡,反应焓变不变,故答案为:向左;不改变;
(3)温度为T℃时,将2a mol H2和 a mol N2放入0.5L密闭容器中,充分反应后测得N2的转化率为50%.则反应的平衡常数可以列出三段式计算平衡浓度,依据平衡常数概念计算:
N2(g)+3H2(g)?2NH2(g)
开始 2amol/L 4amol/L 0
反应 amol/L 3amol/L 2amol/L
平衡 amol/L amol/L 2amol/L
所以化学平衡常数K=
| (2amol/L)2 |
| (amol/L)?(amol/L)3 |
| 4 |
| a2 |
故答案为:
| 4 |
| a2 |
点评:本题考查了反应热、影响化学反应速率的因素,图象分析,化学平衡三段式计算等知识点,中等难度.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
根据物质的熔点、沸点数据,推断错误的是( )
| 晶体 | NaCl | MgO | AlCl3 | SiCl4 | B(硼) |
| 熔点℃ | 801 | 2852 | 180 | -70 | 2300 |
| 沸点℃ | 1465 | --- | 177 | 57 | 2500 |
| A、晶体的沸点CCl4<SiCl4 |
| B、在火山喷出的岩浆,晶出顺序为MgO先于NaCl |
| C、用AlCl3通过电解法冶炼铝 |
| D、硼的硬度大,不溶于水,但能与NaOH溶液反应 |
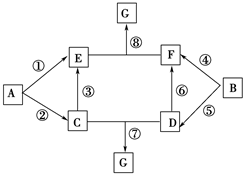 A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).
A~G的转化关系如图所示(部分反应物、产物和反应条件未标出).