��Ŀ����
17�������������ʣ���NaCO3•10H2O���� ��ͭ ������ ��CO2��NaHSO4 ���� ��Ba��OH��2���� �ߺ��ɫ�������������� �ఱˮ ��ϡ���� ��Al2��SO4��3
��1�������������������ε��Тݢ⣨���ţ���
��2����������������������֮��ɷ������ӷ�Ӧ��H++OH-�TH2O��д�������ӷ�Ӧ��Ӧ�Ļ�ѧ����ʽBa��OH��2+2HNO3�TBa��NO3��2+2H2O��
��3��������ˮ���뷽��ʽAl2��SO4��3Al2��SO4��3=2Al3++3SO42-��17.1g������ˮ���250mL��Һ��SO42-�����ʵ���Ũ��Ϊ0.6mol/L��
��4��������Һ�μӵ��ݵ���Һ����ǡ�ó���Ϊֹʱ�����ӷ���ʽH++SO42-+Ba2++OH-�TBaSO4��+H2O��
��5������ᷢ����Ӧ�Ļ�ѧ����ʽΪ��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O����0.6mol����ת��ʱ�����ɵ������״���µ����Ϊ4.48L��
���� ��1������������ӵ���Ϊ�����Σ�
��2��H++OH-�TH2O����ʾ������ǿ�����ǿ�����ʽ���������ǿ�Ӧ���ɿ������κ�ˮ��
��3��������Ϊǿ����ʣ��������������Ӻ���������ӣ����n=$\frac{m}{M}$=cV��������Ũ�ȣ�
��4�������������������ư������ʵ���֮��1��1��Ӧ�����������ǡ�ó�����ȫ��
��5���ڲμӷ�Ӧ��8mol�����У�����ԭ����������ʵ���Ϊ2mol������NO�����ʵ�����2mol��ת�Ƶ�����6mol��
��� �⣺��1�����к���������ӵ�Ϊ�����Σ���NaHSO4 ����͢�Al2��SO4��3���������Σ��ʴ�Ϊ���ݢ⣻
��2��H++OH-�TH2O����ʾ������ǿ�����ǿ�����ʽ���������ǿ�Ӧ���ɿ������κ�ˮ�����Ա�ʾ��������������ķ�Ӧ������ʽ��Ba��OH��2+2HNO3�TBa��NO3��2+2H2O��
�ʴ�Ϊ��Ba��OH��2+2HNO3�TBa��NO3��2+2H2O��
��3����������ǿ����ʣ�����ȫ���룬���뷽��ʽΪ��Al2��SO4��3=2Al3++3SO42-��17.1gAl2��SO4��3����ˮ���250mL��Һ��SO42-�����ʵ���Ϊ$\frac{17.1g}{342g/mol}$=0.05mol��SO42-�����ʵ���Ũ��c=$\frac{n}{V}$=$\frac{0.05mol}{0.250L}$=0.6mol/L��
�ʴ�Ϊ��Al2��SO4��3=2Al3++3SO42-��0.6mol/L��
��4�������������������ư������ʵ���֮��1��1��Ӧ�����������ǡ�ó�����ȫ�����ӷ���ʽ��H++SO42-+Ba2++OH-�TBaSO4��+H2O��
�ʴ�Ϊ��H++SO42-+Ba2++OH-�TBaSO4��+H2O��
��5���ڲμӷ�Ӧ��8mol�����У�����ԭ����������ʵ���Ϊ2mol������NO�����ʵ�����2mol��ת�Ƶ�����6mol������Ӧ��ת����0.6mol���ӣ���������������ʵ�����0.2mol���ڱ�״���µ������0.2mol��22.4L/mol=4.48L��
�ʴ�Ϊ��4.48��
���� ���⿼���˿������ʵķ��ࡢ���ӷ�Ӧ����ʽ����д�����뷽��ʽ����д��������ԭ��Ӧ�����غ���㡢��������ļ����֪ʶ����ȷ����ʸ����Ϥ�����ʵ���Ϊ���ļ��㹫ʽ�ǽ���ؼ������ؿ���ѧ�������ͽ���������������Ŀ�ѶȲ���

������18.0g$��_{��������}^{��������}$����1$\stackrel{��������}{��}$��Һ��$\stackrel{����Cl_{2}}{��}$��Һ��$��_{����}^{���ȡ�����}$����24.0g
����˵������ȷ���ǣ�������
| A�� | ����2�������� | |
| B�� | X�Ļ�ѧʽ���Ա�ʾΪFe3C2 | |
| C�� | ��Һ���п��ܺ���Fe3+ | |
| D�� | X����������Ũ���ᷴӦ��NO2��CO2���� |
| A�� | M���⻯���ˮ��Һ����W��������Һ����Ӧ�õ�W���⻯�˵���ǽ�����M��W | |
| B�� | X��Y�γɵ�ԭ�Ӹ�����Ϊ1��1�ķ����м��Լ��ͷǼ��Լ�֮��Ϊ2��1 | |
| C�� | ZԪ������Ȼ���д�������̬ | |
| D�� | ԭ�Ӱ뾶�Ĵ�С˳��r��W����r��Z����r��Y�� |
| A�� | �������������Һ�еĴ����������ˮ�⣬ͬŨ��ʱǰ�ߵ�ˮ��̶ȱȺ��ߵ�һЩ | |
| B�� | ������ˮ������ˮ��ɱ���嶾ԭ������ͬ�� | |
| C�� | MgO��Al2O3�������������²��ϣ���ҵ�ϲ��õ�����������ұ��þ�������� | |
| D�� | �Ȼ�������Һ�������ɲ����յõ����������� |
| A�� | 10�� | B�� | 9�� | C�� | 8�� | D�� | 7�� |
| A�� | ��������Һ�ܲ��������ЧӦ | B�� | �������ֿ�����ʳƷ�ķ������� | ||
| C�� | ҽ�þƾ�����������ˮ���� | D�� | ���ۡ���֬�������ʿ��ṩӪ�� |
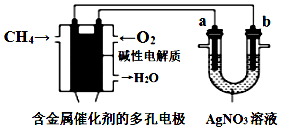
| A�� | ���Ӿ���������b�缫 | |
| B�� | ��b������5.4 gʱ��ȼ�ϵ�ظ�������CH4�����Ϊ140 mL | |
| C�� | ȼ�ϵ����������ӦΪO2+4e-+2H2O�T4OH- | |
| D�� | ��װ�����ڵ����ʱ��һ��ʱ�����������Һ��Ũ�Ȳ��� |
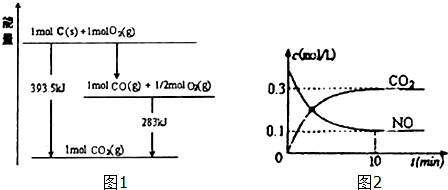
��1����֪һ������C��������O2��g����ȼ�գ�����ܵIJ��P������ϵ��ͼ1��ʾ��
д��CO2��g����C��s����Ӧ����CO��g�����Ȼ�ѧ����ʽCO2��g��+C��s��=2CO��g����H=+172.5kJ/mol��
��2������β�����������з�����Ӧ2NO��g��+2CO��g��?N2+2CO2��g����H��0��һ�������£���ij�ܱպ��������а������1��l����44.8L������״����NO��CO������壬����������Ӧ��ijͬѧ���ݷ�Ӧ�����е��й����ݻ�������ͼ2��ʾ���ߣ�
�����й���������Ӧ���̵�������ȷ����AD����д��ĸ���ţ���
A�������������䣬�����������H��ֵ����
B����ʱ��ȥ������̼����Ӧ������Ӧ���ʼӿ�
C��NO��CO��N2��CO2Ũ�Ⱦ����ٱ仯��˵��δ�ﵽƽ��״̬
D����������ƽ����Է����������ٸı䣬֤����Ӧ�ﵽ��ѧƽ��״̬
��ǰ10min��CO��ƽ����Ӧ����Ϊ0.03mol/��L•min������ƽ��ʱNO��ת����Ϊ75%����ʹ����ƽ����ϵ��$\frac{n��C{O}_{2}��}{n��NO��}$����Ĵ�ʩ�н����¶Ȼ��ѹ������CO�����ʵ��������ϵ�з����N2����дһ������
��3����֪���������ˮ�еĵ���ƽ�ⳣ����25�棩���±�����λʡ�ԣ���
| ������� | H2CO3 | NH3•H2O |
| ����ƽ�ⳣ�� | Ka1=4.2��10-7��������Ka2=5.6��10-11 | 1.7��10-5 |
�ڳ����£����ij̼�����ϵ�pH=6���������$\frac{n��C{O}_{3}^{2-}��}{n��HC{O}_{3}^{-}��}$=5.6��10-5��