题目内容
10.为了除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+,最适合的氧化剂是( )| A. | H2O2水溶液 | B. | KMnO4溶液 | C. | Cl2水溶液 | D. | HNO3溶液 |
分析 除去硫酸铜溶液中含有的Fe2+杂质,先加入合适的氧化剂使Fe2+氧化为Fe3+,且不能引入新杂质,然后调节pH使铁离子转化为沉淀,过滤可除杂,以此来解答.
解答 解:B、C、D中氧化剂均可氧化Fe2+,但引入新杂质不易除去,只有A中过氧化氢的还原产物为水,符合题意,
故选A.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、提纯时不能引入新杂质为解答的关键,侧重分析与实验能力的考查,注意氧化还原反应的应用,题目难度不大.

练习册系列答案
 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
2.维生素C的结构简式如图所示.则有关它的叙述中错误的是( )
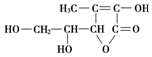

| A. | 易发生氧化及加成反应 | B. | 在碱性溶液中能稳定地存在 | ||
| C. | 能与乙酸发生酯化反应 | D. | 是一个环状的酯类化合物 |
1.将一定质量的镁铜合金加入到l00mL某浓度HNO3中,两者恰好反应,产生NO2和NO气体,反应后向所得溶液中加入4mol•L-1的NaOH溶液至恰好沉淀完全,测得所得沉淀过滤干燥后质量增加了10.2g,则下列说法不正确的是( )
| A. | 开始加入合金的总物质的量为0.3mol | |
| B. | 生成的气体在标准状况下大于4.48L | |
| C. | 所加NaOH溶液体积为150mL | |
| D. | 原硝酸浓度为6mol•L-1 |
18.关于化学能与其他能量相互转化的说法正确的是( )

| A. | 化学反应中能量变化的主要原因是化学键的断裂与形成 | |
| B. | 铝热反应属于放热反应,反应物的总能量比生成物的总能量低 | |
| C. | 图I所示的装置可以实现将化学能转变为电能 | |
| D. | 图II所示的反应为吸热反应 |
5.?下列物质转化常通过加成反应实现的是( )
| A. |  → → | B. | CH2=CH2→CH2BrCH2Br | ||
| C. | ?CH4→CH3Cl | D. | CH3CH2OH→CH3CHO |
2.下列关于苯乙炔的说法错误的是( )
| A. | 该分子有8个σ键,5个π键 | |
| B. | 该分子中碳原子有sp和sp2杂化 | |
| C. | 该分子存在非极性键 | |
| D. | 该分子中有8个碳原子在同一平面上 |
19.下列各组物质中属于同分异构体的是( )
| A. | H2O和D2O | B. | 淀粉和纤维素 | C. |  和 和 | D. | 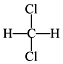 和 和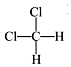 |
20.NA为阿伏加德罗常数的值.下列说法错误的是( )
| A. | 0.1 mol 的11B中,含有0.6NA个中子 | |
| B. | 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA | |
| C. | 28g乙烯和环丁烷(C4H8)的混合气体中含有共用电子对的数目为3NA | |
| D. | 标准状况下,5.6L氯气与足量的镁粉反应,转移的电子数为0.5NA |
 的离子方程式:2ClO﹣+CO2+H2O═2HClO+CO32﹣
的离子方程式:2ClO﹣+CO2+H2O═2HClO+CO32﹣