题目内容
2.将下列性质的代号,填入各小题后面对应的括号中:A.脱水性; B.强酸性; C.难挥发性; D.氧化性; E.吸水性
(1)在稀硫酸中放入铝片就产生H2.B
(2)浓硫酸敞口久置会增重.E
(3)把浓H2SO4滴在纸上,纸变黑.A
(4)用稀硫酸清洗金属表面的氧化物.B
(5)把木炭放入热的浓硫酸中时,有气体放出.D
(6)在常温下可以用铁、铝制容器盛装冷的浓硫酸.D.
分析 浓硫酸具有吸水性,可用作干燥剂,具有脱水性,可使蔗糖碳化而变黑,具有强氧化性,可与不活泼金属在加热条件下反应,与铝、铁等金属在常温下发生钝化反应,浓硝酸氧化性大于稀硝酸,以此解答该题.
解答 解:(1)在稀H2SO4中放入铝片就产生H2,体现硫酸的酸性,故答案为:B;
(2)浓硫酸具有吸水性,则浓H2SO4敞口久置会增重,故答案为:E;
(3)在烧杯中放入蔗糖,滴入浓H2SO4变黑,浓硫酸夺取蔗糖分子结构中的氧原子和氢原子生成水,体现脱水性,故答案为:A
(4)用稀硫酸清洗金属表面的氧化物,表现了硫酸的酸性,故答案为:B;
(5)把木炭放入热的浓硫酸中时,有气体放出,生成二氧化碳和二氧化硫,浓硫酸表现强氧化性,故答案为:D;
(6)在常温下可以用铁、铝制容器盛装冷的浓硫酸,原因是浓硫酸与铁、铝发生钝化反应,浓硫酸表现强氧化性,故答案为:D.
点评 本题综合考查硫酸的性质,为元素化合物知识常见题型和高频考点,难度中等,注意相关基础知识的积累.

练习册系列答案
相关题目
12.化学与生活、生产、能源等密切相关,下列叙述不正确的是( )
| A. | 利用催化剂可将汽车尾气中的NO、CO转化为无毒的气体 | |
| B. | 化石燃料的过量使用加剧了雾霾天气及空气中的PM2.5 | |
| C. | 小苏打是制作馒头和面包的膨松剂,还是治疗胃酸过多的一种药剂 | |
| D. | 蛋白质溶液中加入饱和Na2SO4溶液或CuSO4溶液,析出固体原理相同 |
13.下列物质中,含有共价键的离子化合物是( )
| A. | N2 | B. | NH4Cl | C. | HCl | D. | NaCl |
10.10.0mL 某气态烃在 50.0mL O2中充分燃烧,得到液态水和35.0mL 的气体混合物(所有气体的体积都是在同温同压下测得的),则该气态烃可能是( )
| A. | CH4 | B. | C2H6 | C. | C3H8 | D. | C4H10 |
17. 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.
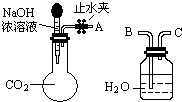
(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应.将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是水沿导管由广口瓶进入烧瓶(或:水倒吸进入烧瓶),反应的离子方程式是2OH-+CO2=CO32-+H2O(或CO2+OH-=HCO3-).若其它操作不变,将A与C连接,可观察到的现象是广口瓶中的长导管口有气泡产生.
(2)向100mL2mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3g白色固体,该白色固体的组成是NaOH和Na2CO3(写化学式).
设计实验确认该白色固体中存在的阴离子,试完成下列方案.
(3)在标况下,将4.48L CO2气体通入300mL 1mol/L 的NaOH的稀溶液中,写出该反应的离子方程式(用一个离子方程式表示)2CO2+3OH-=CO32-+HCO3-+H2O.
 纯碱、烧碱等是重要的化工原料.
纯碱、烧碱等是重要的化工原料.(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应.将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是水沿导管由广口瓶进入烧瓶(或:水倒吸进入烧瓶),反应的离子方程式是2OH-+CO2=CO32-+H2O(或CO2+OH-=HCO3-).若其它操作不变,将A与C连接,可观察到的现象是广口瓶中的长导管口有气泡产生.
(2)向100mL2mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3g白色固体,该白色固体的组成是NaOH和Na2CO3(写化学式).
设计实验确认该白色固体中存在的阴离子,试完成下列方案.
| 实验操作 | 实验现象 | 结论 |
| ①取少量白色固体于试管中,加足量水溶解,再加足量BaCl2溶液 | 产生白色沉淀 | 有CO32- |
| ②过滤,取2mL滤液于试管中 | ||
| ③滴加酚酞 | 溶液变红 | 有OH- |
7.分别用一种试剂将下列物质中混入的少量杂质除去(括号内为混入的杂质)
| 物质 | 需加入的试剂 | 有关离子方程式 |
| FeSO4 (Fe2(SO4)3) | ||
| Mg(Al) | ||
| CO2 (HCl) | ||
| SiO2(CaCO3) | . |
14.有机化合物中ω(C)=60%,ω(H)=13.33%,0.2mol该有机物的质量为12g,则它的分子式为( )
| A. | CH4 | B. | C3H8O | C. | C2H4O2 | D. | CH2O |
9.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 1 mol OD-离子含有的质子、中子数均为10NA | |
| B. | 标准状况下,4.48 L己烷含有的分子数为0.2NA | |
| C. | 标准状况下,6.72LNO2与水反应消耗的氧化剂分子数为0.2NA | |
| D. | 丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA |
10.下列反应中,属于取代反应的是( )
| A. | CH4$\stackrel{高温}{→}$C+2H2 | B. | 2HI+Cl2=2HCl+I2 | ||
| C. | CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | D. | C2H6+Cl2$\stackrel{光}{→}$C2H5Cl+HCl |