题目内容
3.浅绿色的硝酸亚铁溶液存在如下平衡:Fe2++2H2O?Fe(OH)2+2H+,若在此溶液中加入盐酸,则溶液的颜色( )| A. | 变深 | B. | 变浅 | C. | 变黄 | D. | 不变 |
分析 此溶液中加入盐酸,发生3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,以此来解答.
解答 解:此溶液中加入盐酸,发生3Fe2++4H++NO3-=3Fe3++NO↑+2H2O,且Fe2++2H2O?Fe(OH)2+2H+逆向移动,c(Fe2+)减小,c(Fe3+)增大,溶液变为黄色,
故选C.
点评 本题考查化学平衡及氧化还原反应,为高频考点,把握硝酸盐在酸性条件下的强氧化性为解答的关键,侧重分析与应用能力的考查,注意不能单纯的考虑平衡移动,题目难度不大.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
13.下列有关物质分类或归类中,正确的是( )
①混合物:盐酸、漂白粉、氯水、水玻璃 ②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、生石膏、冰醋酸、氨水 ④酸性氧化物:SiO2 Mn2O7 N2O5 Cl2O7 .
①混合物:盐酸、漂白粉、氯水、水玻璃 ②化合物:CaCl2、NaOH、HCl、HD
③电解质:明矾、生石膏、冰醋酸、氨水 ④酸性氧化物:SiO2 Mn2O7 N2O5 Cl2O7 .
| A. | ①④ | B. | ②③ | C. | ③④ | D. | ③ |
14.下列物质溶于水时会破坏水的电离平衡,且属于电解质的是( )
| A. | 氯气 | B. | 氨气 | C. | 碘化钾 | D. | 碳酸氢钠 |
11.为了测定K2CO3和NaHCO3混合物的组成,某学生每次称取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的Ba(OH)2溶液,每次实验均充分反应,实验结果记录如下
请回答下列问题:
(1)第二次实验中产生沉淀的质量是2.758g;
(2)混合物中K2CO3和NaHCO3的物质的量之比为5:2.
| 实验次数 | 混合物的质量/g | 所加Ba(OH)2溶液的体积/L | 测得沉淀的质量/g |
| 1 | 0.858 | 0.5 | 1.379 |
| 2 | 1.716 | 0.5 | |
| 3 | 2.574 | 0.5 | 4.137 |
| 4 | 3.432 | 0.5 | 5.516 |
| 5 | 4.290 | 0.5 | 5.516 |
| 6 | 5.148 | 0.5 | 5.516 |
(1)第二次实验中产生沉淀的质量是2.758g;
(2)混合物中K2CO3和NaHCO3的物质的量之比为5:2.
18.中华民族有着光辉灿烂的发明史,下列发明创造不涉及氧化还原反应的是( )
| A. | 用胆矾炼铜 | B. | 用铁矿石炼铁 | ||
| C. | 用黑火药开山炸石 | D. | 打磨磁石制指南针 |
15.Na2CO3、NaHCO3、CaO和NaOH组成的混合物27.2g,溶于足量水并充分反应后,溶液中Ca2+、CO32-、HCO3-全部转化为沉淀,将反应容器内水分蒸干,最后得到白色固体29.0g.则原混合物中Na2CO3的质量是( )
| A. | 10.6 g | B. | 5.3 g | C. | 15.9 g | D. | 5.6 g |
12.在花瓶中插上一束美丽的鲜花,将会给你紧张而又忙碌的学习、生活带来轻松和愉悦的心情.可是过不了几天,花儿就会枯萎.如果在花瓶中加入“鲜花保鲜剂”,就会延长鲜花的寿命.表是1L“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是A(填字母).
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中的K+的物质的量浓度约为(阿司匹林中不含K+)8.91×10-3mol/L
(3)配制上述1L“鲜花保鲜剂”所需的仪器有:量筒、烧杯、玻璃棒、托盘天平、药匙、胶头滴管,1000mL容量瓶.(填所缺仪器的名称).
(4)在溶液配制过程中,下列操作对配制结果没有影响的是BD(填字母).
A.定容用胶头滴管加水时,仰视观察溶液凹液面与容量瓶刻度线相切
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)实验室用固体加热制氨气的化学反应方程式为:2NH4Cl+Ca(OH)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
(6)若将收集到的氨气溶于水配成100mL的溶液,所得氨水中NH3物质量浓度(不考虑NH3与H2O的反应)为0.3mol•L-1,则需要氨气的体积为672mL(标准状况).
| 成 分 | 质 量(g) | 摩尔质量(g/mol) |
| 蔗糖 | 50.00 | 342 |
| 硫酸钾 | 0.50 | 174 |
| 阿司匹林 | 0.35 | 180 |
| 高锰酸钾 | 0.50 | 158 |
| 硝酸银 | 0.04 | 170 |
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中的K+的物质的量浓度约为(阿司匹林中不含K+)8.91×10-3mol/L
(3)配制上述1L“鲜花保鲜剂”所需的仪器有:量筒、烧杯、玻璃棒、托盘天平、药匙、胶头滴管,1000mL容量瓶.(填所缺仪器的名称).
(4)在溶液配制过程中,下列操作对配制结果没有影响的是BD(填字母).
A.定容用胶头滴管加水时,仰视观察溶液凹液面与容量瓶刻度线相切
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(5)实验室用固体加热制氨气的化学反应方程式为:2NH4Cl+Ca(OH)$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O
(6)若将收集到的氨气溶于水配成100mL的溶液,所得氨水中NH3物质量浓度(不考虑NH3与H2O的反应)为0.3mol•L-1,则需要氨气的体积为672mL(标准状况).
13.镁铝组成的混合物平均分成两份,一份与足量氢氧化钠溶液反应,另一份与足量稀盐酸反应,产生氢气的质量前者是后者的二分之一,则混合物中镁铝的质量比是( )
| A. | 1:1 | B. | 3:4 | C. | 4:3 | D. | 3:2 |
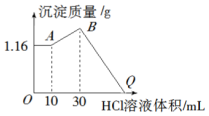 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示.
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示.